丘脑胶质母细胞瘤生存期有多久?较大水平手术切除和辅助技术可好转预后
发布时间:2021-11-26 14:25:34 | 阅读:次| 关键词:
- [案例]16岁基底节胶质瘤患者赴德手术,近全切功能区脑瘤
- [案例]儿子因脑干出血病危,两次120转运,为何医生说法截然不
- [案例]天坛医院手术随访|"无症状"脑瘤需手术吗?术后她实
- [案例]JNS发表德国巴特朗菲教授135例脑干脑桥海绵状血管瘤手术
- [案例]面部“刀割”之痛不再:INC国际福教授全切岩斜区脑膜瘤
- [案例]研究发现低级别胶质瘤“早期手术”的生存益处
丘脑胶质母细胞瘤生存期有多久?丘脑位于大脑深处,靠近重要的神经结构。较大切除治疗胶质母细胞瘤(GBM)的重要性已经报道了许多研究。然而,丘脑肿瘤的切除与高速率发病率和死亡率,从而丘脑胶质母细胞瘤的较大切除很少尝试,和较大手术切除的作用仍不清楚。在丘脑胶质母细胞瘤治疗过程中,通常进行活检以确认病理诊断和分子特征,而手术切除仍然具有挑战性。此外,已经报道了合适手术切除的方法,其中一些报道包括对手术方法的描述。
2021年2月新近发表的论文《Maximal surgical resection and adjuvant surgical technique to prolong the survival of adult patients with thalamic glioblastoma》中通过临床研究证明了手术切除在成人丘脑胶质母细胞瘤(GBM)治疗中的作用,并确定较大顺利切除的手术技术所产生的影响。
丘脑胶质母细胞瘤的治疗策略
在怀疑丘脑胶质母细胞瘤的情况下,手术切除是我们医院的优选治疗方法。如果可能,手术的目的是获得总体全切除。在预期出现严重神经系统并发症、怀疑皮质脊髓束(CST)损伤或可能发生脑干损伤或血管损伤的情况下进行次全切除。活检是心室壁强化、软脑膜强化或远处多发强化病变患者的治疗选择。病理诊断确诊后,本研究全部患者均接受胶质母细胞瘤标准治疗(同步放化疗和替莫唑胺化疗)
丘脑胶质母细胞瘤的辅助手术技术
术前导航MRI、弥散张量纤维束成像(DTI)、增强型计算机断(CT)常规进行并融合在一起。在硬脑膜完全打开之前,将尾弹通过小硬脑膜切口(<5 mm)的切口插入肿瘤靶标,其主要目标区域是皮质脊髓束和中脑,在手术过程中难以区分。在融合图像中标记了靶标插入的目标点。在手术过程中,使用这些靶标,我们能在显微镜下确认目标病变并将融合图像与目标点进行比较。由于手术过程中肿瘤体积缩小,肿瘤及其周围环境发生了改变;因此,术中进行CT以识别脑病灶相对于融合图像的变化。5-ALA(5-氨基乙酰丙酸)用于区分全部手术切除病例中的肿瘤病变。经颅运动诱发电位(MEP)和单较直接皮层下刺激(DSS)用于确认术中功能状态和CST的位置。在整个皮层手术过程中,每5分钟以60~100 mA监测经颅MEP。DSS以10 mA启动,并随着刺激器接近CST而降低至6 mA。如果患者状态允许,则在患者清醒时进行清醒手术,以检查患者术中功能状态。
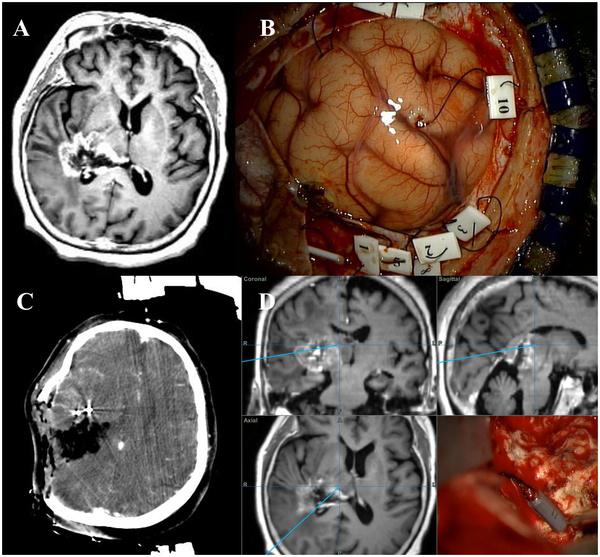
右侧后丘脑胶质母细胞瘤的术前磁共振图像,横向扩展(A)。尾弹插入目标区域(B)。在手术过程中,利用术中计算机断层扫描图像和尾弹技术进行脑移位的调整和目标病灶的确认(C,D)。
丘脑胶质母细胞瘤的手术入路
手术入路的选择是根据肿瘤中心的位置和相邻的皮质脊髓束。考虑到肿瘤扩展的模式和CST的位置,选择了从皮质到肿瘤的较短通道。当肿瘤位于丘脑前外侧或后外侧并向上外侧方向延伸时,选择经皮质入路。当肿瘤位于后外侧丘脑时,选择经皮层-经脑室入路。当肿瘤位于丘脑内侧和后部时,选择了半球间经胼胝体入路,而外侧丘脑病变则选择了经外侧裂-经岛叶入路。对于丘脑后下部和内侧后下部病变,采用枕部经小脑幕入路。改良的外侧眶上(MLSO)入路用于治疗前丘脑肿瘤。
临床结果
为了评估手术切除与活检相比的临床疗效,我们估计了三组之间OS和PFS率的差异:手术切除(n=19)、医生选择的活检(n=17)和患者选择的活检(n=6)。手术切除组显示出良好的OS(中位数:676天,p=0.001)(图4A)和PFS(中位数:328天,p=0.001)(图4B)与所述活检组(医生选择活组织检查,位OS相比:240天,中位PFS:134天;选择活检的患者,中位OS:212天,中位PFS:118天)
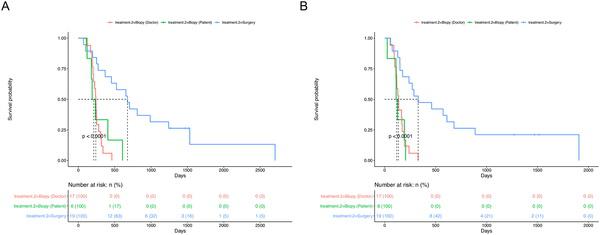
手术切除和活检组的生存分析。A.与根据治疗标准接受活检的患者(医生选择活检组)或选择活检的患者(患者选择活检组)相比,接受手术切除的患者的平均总生存时间(OS)更长(p<0.001)。B.与选择活检组的医生或选择活检组的患者相比,手术切除组的无进展生存期更长。
此外,研究专家还表示,手术切除组与活检组在运动相关的神经系统并发症如运动无力、感觉障碍、视力障碍、认知恶化和KPS恶化方面无显着差异
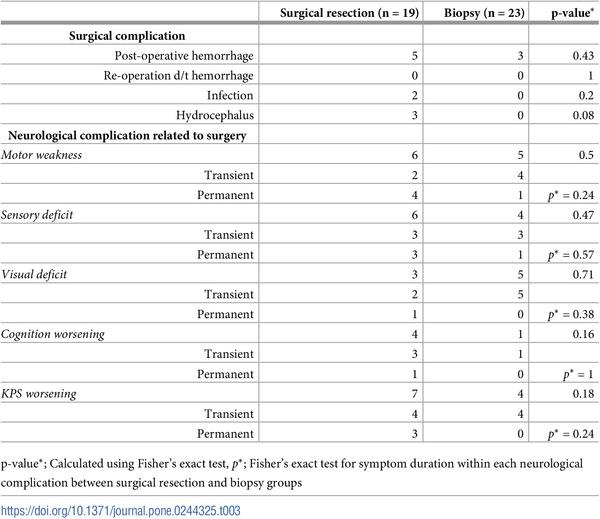
手术切除组和活检组之间手术和神经系统并发症的分布图
辅助手术技术和手术入路
全部手术切除病例均采用导航MRI、DTI、增强CT、术中CT、尾弹、经颅MEP、DSS,以及荧光染料(5-氨基乙酰丙酸)。在患者状态和手术位置允许的情况下,有5例患者进行了清醒手术。总共应用了六种手术方法。经皮层经脑室入路是较常用的,适用于外侧后下和后上丘脑病变。5例采用经皮层入路,应用于丘脑前、外侧和外侧后部病变。4例采用半球间经胼胝体入路,应用于内侧和后上方病变。2例采用枕部经小脑幕入路,应用于内侧后下方病变。一例外侧丘脑病变采用经外侧裂-经岛叶入路。MLSO入路用于治疗丘脑前部病变的一例。根据手术方法,OS(p=0.69)和PFS(p=0.55)没有显着差异。
讨论
丘脑胶质母细胞瘤中对比度增强病变的较大切除是困难的。在Esquenazi等人的研究中,全部手术病例均进行次全切除。在Kiran等人的一项研究中,12名丘脑GBM患者中有7例实现了GTR或接近完全切除,这是一个相对较高的比率。在本研究中,19名接受手术切除的患者中有11名实现了GTR。然而,OS(p=0.33)和PFS(p=0.38)在GTR和STR组之间。在评价术后结果时,STR定义为80%~全切切除;因此,当比较STR与活检的结果时,手术切除组的OS和PFS明显长于活检组。因此,80%以上的较大切除被认为比非较大切除具有更好的生存获益。即使在STR组中,较好尝试的手术治疗,因为与活检组(S5C和S5D图)相比,它显示出OS(p=0.0017)和PFS(p=0.0084)的显着差异。
根据FLAIR图像,本研究中没有GTR病例。然而,很难去除FLAIR图像中的全部高信号病变,因为这些病变遍布丘脑或围绕脑干和CST。尽管并非全部FLAIR信号改变的病灶都可以切除,但较大水平切除对比增强病灶可以提高丘脑胶质母细胞瘤患者的生存率。
除了较大限度地切除肿瘤,功能保留也很重要。丘脑与各种身体功能有关,丘脑胶质母细胞瘤手术切除会导致严重的神经功能缺损。丘脑胶质母细胞瘤手术并发症也与预后不良有关。手术时难以区分丘脑胶质母细胞瘤的边缘与正常组织,手术中发生结构移位时更难以判断肿瘤边界。目前的研究表明,辅助手术技术,包括使用尾子弹和术中CT的,能够帮助划定靶病变。当手术中遇到边界不清的子弹时,子弹不仅可以显示目标病变,还可以显示结构的运动程度。此外,术中CT可用于确认现有术前MRI图像的变化,并通过检查子弹位置来纠正位置。虽然术中MRI在丘脑GBM手术中更有用,这里仅采用术中CT,难以确认T2信号改变病灶或FLAIR高信号病灶。将尾弹插入目标病灶(T2或FLAIR信号改变病灶)后,通过术前和术中图像的比较,有助于调整病灶的术中位移。此外,荧光染料用于区分全部手术切除病例和清醒手术中的肿瘤病变,有助于预防神经系统并发症在五种情况下进行。荧光染料(5-ALA)的有用性已经在许多论文中介绍过,许多机构将5-ALA用于胶质母细胞瘤手术。我们还使用5-ALA作为帮助区分肿瘤病变的辅助手段。
由于丘脑胶质母细胞瘤手术较有可能诱发高发病率,因此手术后患者的功能状态较为重要。如果手术能提高生存率,但功能缺陷很严重,手术的作用就很有限了。在接受手术切除的19名患者中,18名能够维持或好转其功能状态,KPS评分超过60,而没有出现严重的神经功能缺损。手术切除组19例患者中,有1例KPS评分恶化超过20分且小于60分,因此手术切除组与活检组KPS恶化无显着差异(p=0.18)。我们发现使用手术切除治疗成人丘脑GBM可延长患者的生存期并保持患者的体能状态。
在我们的研究中,丘脑肿瘤手术入路选择的较重要方面是保存正常的大脑结构。我们选择通过准确识别与肿瘤起源相对应的丘脑震中以及与重要连接神经结构的位置关系,可以较大限度地减少对CST和其他结构的损害的方法。Ranger-Castilla等人。已经为六个不同区域提供了六种的手术方法的分类。在此分类的基础上,根据肿瘤起源位置和扩展模式选择每种方法。如果可能,较好避免在手术通道中进行CST,并选择一种对语言皮层和视觉通路损伤较小的方法。根据手术方法,OS(p=0.69)和PFS(p=0.55)没有差异。此外,丘脑GBMs是深部肿瘤;因此,根据外科医生的选择选择不同的方法来防止手术过程中的牵拉损伤。对于后部位置,D'Angelo等人后侧半球间入路,而Steiger等人优选对侧幕下小脑上入路治疗枕叶内侧。由于视野相对较宽,我们更喜欢枕部经小脑幕入路,因为可以预期使用自然重力产生回缩效果,从而避免在内侧后下丘脑病变的情况下对视野造成损害。基于这些策略选择了手术入路,本研究取得了良好的效果。每种入路的手术切除程度和神经结构损伤的可能性可能存在显着差异,因此应在考虑手术目的后选择入路。
这是一项具有回顾性设计的观察性研究。活检组和手术切除组之间的比较存在选择偏倚,因此我们进行了额外的亚组分析。由于本研究仅包含相对少量的手术切除病例,因此需要进一步研究更多的病例。H3K27m突变是丘脑胶质母细胞瘤的一个重要预后因素,但它没有被包括在本研究中,因为它只在我们机构的少数病例中进行了测试。在未来的研究中应该包括更多的分子诊断。
结论
对于丘脑胶质母细胞瘤患者,选择合适的手术切除候选者很重要。如果没有心室壁增强病灶或没有多发病灶,当较大手术切除率超过80%时,可以预期比单独活检有更长的生存期。使用尾弹和术中影像方式有助于降低手术发病率,通过仔细监测如MEP和DSS来检查神经生理状态很重要。手术入路可根据肿瘤震中位置及邻近的CST进行选择。
参考文献:https://doi.org/10.1371/journal.pone.0244325

- 所属栏目:胶质瘤
- 如想转载“丘脑胶质母细胞瘤生存期有多久?较大水平手术切除和辅助技术可好转预后”请务必注明来源和链接。
- 网址:https://www.incsg.com/jiaozhiliu/1329.html
- 更新时间:2021-11-26 14:22:01







