视路胶质瘤能活多久?27年无复发的背后,手术入路的选择艺术
发布时间:2026-02-22 13:34:04 | 阅读:次| 关键词:视路胶质瘤能活多久?27年无复发的背后,手术入路的选择艺术
- [案例]年纪大了,听力下降很正常?小心脑干被听神经瘤挤压变
- [案例]INC国际Rutka教授团队发表成果助力儿童胶质瘤免疫治疗
- [案例]1岁女孩因走路不稳查出脑瘤,首次开颅后无法走路,二次
- [案例]基底节区海绵状血管瘤患者从瘫痪到露营:68岁女性治疗实
- [案例]15分钟就决定开颅手术:为什么我一定要切除这个“暂时安
- [案例]开颅也看不见的脑瘤如何应对?国际专家运用“可视化技
视路胶质瘤患者的生存期究竟有多长?一项研究系列的平均随访期为5.5 ± 4.16年。由于许多患者来自其他国家,因此随访期相对有限。在该系列中,一名14岁女性患儿是随访时间最长的患者。在显微手术切除鞍上毛细胞型星形细胞瘤27年后,重复磁共振扫描证实该患者无肿瘤复发,且在低剂量替代药物治疗下,其临床及内分泌状况保持优良。她与其余接受了肿瘤全切除的患者一起,属于视路-下丘脑胶质瘤患者中,在显微外科治疗后获得良好预后的群体。
视路-下丘脑胶质瘤患者的生存期与其病理类型、手术切除程度及综合治疗策略密切相关。在INC国际神经外科专家Helmut Bertalanffy(巴特朗菲)教授与Concezio Di Rocco教授共同发表的《Surgical Treatment of Optic Pathway Hypothalamic Gliomas》研究中,对这类疾病的诊疗策略进行了系统阐述。其中巴教授手术的系列研究中,一名14岁患者获得了术后27年无复发的长期疗效。

图:INC国际儿童神外大咖Concezio Di Rocco教授主编的《Advances and Technical Standards in Neurosurgery 》是神经外科领域颇具影响力的系列丛书,每年出版一卷,收录该领域最新的技术进展和权威综述,对临床医生和研究人员有很高的参考价值。
视路胶质瘤概述与巴教授治疗策略解析
视路-下丘脑胶质瘤好发于青少年,肿瘤常沿视觉通路广泛生长,可累及视神经、视交叉、视束、下丘脑-垂体轴、第三脑室、Willis环及周围重要脑组织。尽管主流治疗推荐化疗,巴特朗菲教授二十年来坚持采用积极的手术策略,为多数患者实现了肿瘤全切。以下将重点解析巴教授对该疾病的手术入路选择。
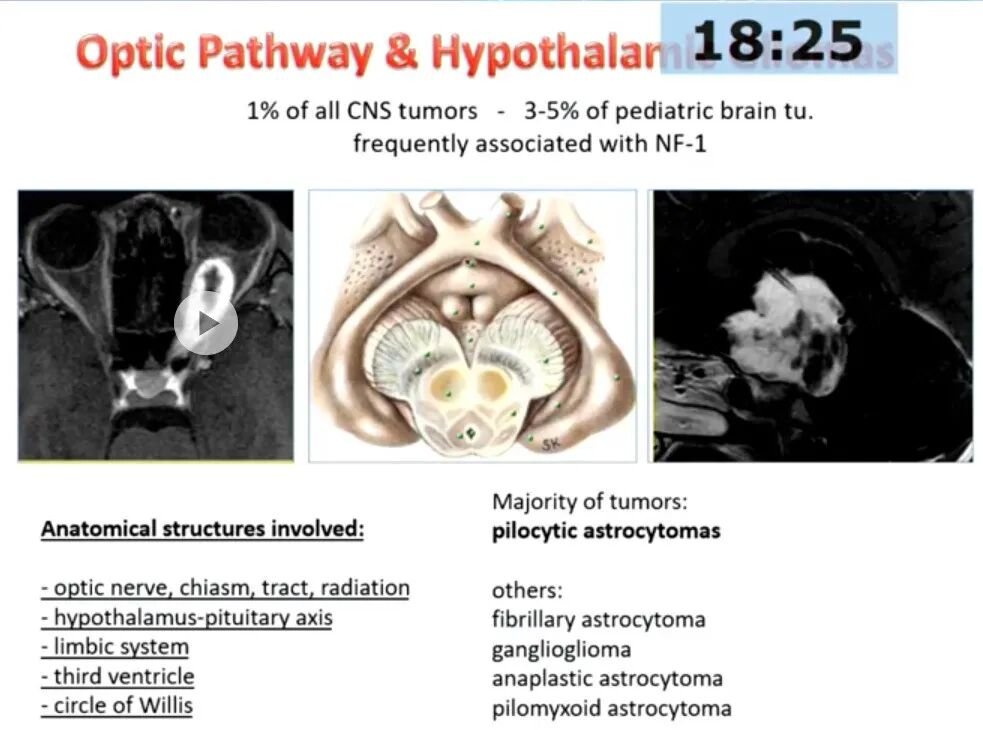
图:视路-下丘脑胶质瘤解剖结构示意图,显示其可累及视神经、视交叉、下丘脑、第三脑室及Willis环等重要区域。
手术目标设定
对于有症状的患者,手术的主要目标是有效阻断肿瘤对视路系统和/或下丘脑造成的渐进性损害的病理机制。因此,手术的首要目标是通过在安全范围内尽可能多地切除肿瘤体积,实现对视神经或视交叉的充分减压,并争取达到全切或至少近全切除,以避免肿瘤复发。同时,手术也旨在保护相关解剖结构的完整性和生理功能,特别是视路系统与下丘脑-垂体轴,并且至关重要的是获得精确的组织病理学诊断。
对于预计无法完全切除的弥漫性肿瘤的低龄患儿,肿瘤减容(近全切除或次全切除)是一种合理的治疗选择,因为其有望在患儿达到可接受放射治疗的年龄前维持视力与内分泌功能。同样,对于体积巨大且有症状的肿瘤,若全切除可能以双侧视力丧失或其他严重神经或内分泌功能缺损为代价,则计划性部分肿瘤切除即为手术目标。
对于已单侧失明的眶内视神经胶质瘤患者,手术的主要目标不仅包括切除肿瘤累及的视神经,还需确保肿瘤(尤其是近端区域)的完全切除,以防止残余肿瘤向视交叉内增殖。
术前准备要点
高质量神经影像学检查是制定恰当手术方案不可或缺的基础。此外,患者术前需接受近期眼科检查,除常规血液检测外还需完成全套激素水平评估,以便术后即刻优化替代治疗方案。
鉴于视路-下丘脑胶质瘤紧邻重要神经血管结构、与视交叉及下丘脑边界不清、具有较高的视力丧失或严重下丘脑功能障碍手术风险,且患者预期生存期较长需终身治疗与随访,此类肿瘤属于极具挑战性的病变。因此,相当数量的神经外科、神经内科、神经肿瘤科及小儿神经科医师将视路-下丘脑胶质瘤视为“不可手术”的肿瘤。
必须向转诊医师、患者及其家属明确阐述不同的治疗策略。此外,除肿瘤局限于视神经的患者外,需强调下丘脑区肿瘤切除术后可能立即出现暂时性下丘脑功能失衡,且多数情况下需行激素替代治疗。同时,需确保患者及其亲属理解:这种术后早期下丘脑功能障碍可能导致具有潜在危险的血钠水平波动,这种不稳定状态可能持续至术后3周,且此类电解质紊乱是下丘脑区域手术可预见的已知并发症。
手术入路个体化设计
手术入路根据每例肿瘤的形态学特征进行个体化设计,主要依据三维MRI显示的确切病灶位置、大小及范围进行选择。原则上,对下丘脑肿瘤采用与其他鞍上肿瘤相似的手术入路,包括前外侧入路(经外侧裂)或中线入路(额底纵裂)。眶内肿瘤的显露始终需要充分的眶壁骨质暴露。
仅一例24岁男性患者的视路-下丘脑胶质瘤延伸至第三脑室,采用高位额部矢状窦旁开颅,经纵裂-胼胝体-穹窿旁入路,经右侧侧脑室显露肿瘤。其余55例患者均采用外侧或中线手术入路。
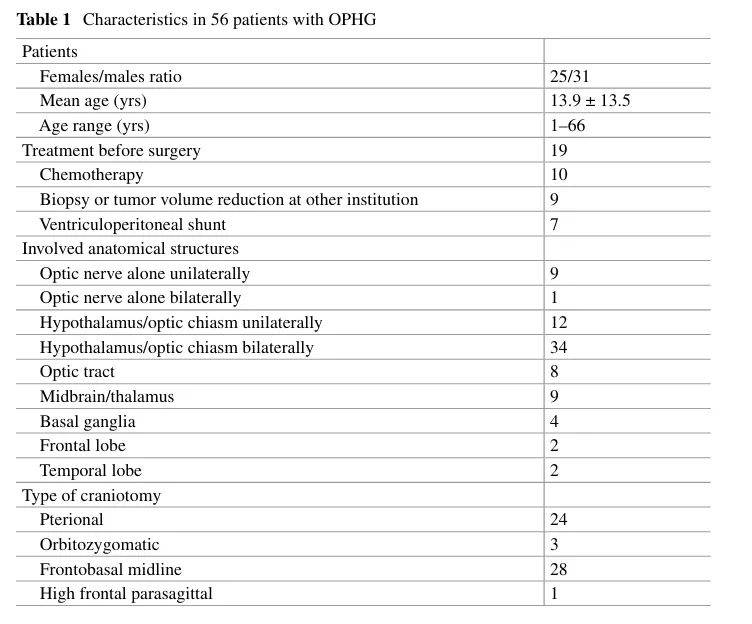
表:56例视路-下丘脑胶质瘤患者特征表,包含性别比例、平均年龄、既往治疗史、累及解剖结构及开颅类型等数据。
翼点开颅联合经外侧裂入路技术解析
对于此外侧入路,采用仰卧位,抬高患者下肢及上半身,将头部向对侧旋转约45度并略向后伸展。出于美观考虑,应注意将皮肤切口设计在发际线后方。对于既往接受过手术的患者,尽可能沿原手术瘢痕切开皮肤。同样,对于额颞区域有分流装置部件的患者,会将皮肤切口标记在更靠前的位置,以避免暴露并可能损伤分流系统。
以利于术后美观缝合的方式切开颞肌。通常,两到三个骨孔足以抬起标准的翼点骨瓣。随后,使用金刚钻磨除蝶骨小翼、眶顶及至少部分眶外侧壁。常规切开脑膜-眶带并切除前床突,从而完全暴露视神经管的硬膜鞘,其近端与额叶硬脑膜(镰状韧带)相连,远端与眶骨膜相连。
通常,如此广泛的眶周暴露仅对眶内肿瘤患者是必要的。对于其他患者,较少暴露眼眶,但总会切除前床突并从硬膜外暴露视神经管,以便更好地进行硬膜内探查或手术处理同侧管内段视神经。眶内视神经的暴露可选择从上路进入,即经上直肌内侧进入眼眶;或从外侧进入,即在上直肌与外直肌之间操作。
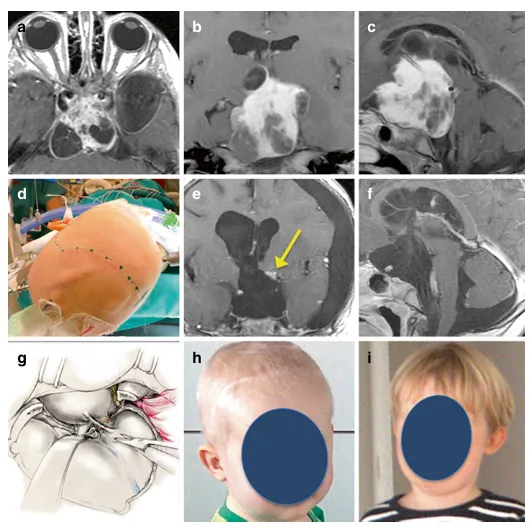
图:一名2岁男性患儿鞍上一囊实性、显著强化的占位性病变延伸至左侧颞叶,经左翼点开颅入路行肿瘤全切除术。术后MRI证实肿瘤全切,患儿状况良好。
眶颧开颅联合经外侧裂入路技术解析
眶颧暴露是翼点开颅的一种扩展变异。虽然患者体位和皮肤切口与翼点开颅相同,但骨窗暴露范围还包括了颧弓和颧骨后部。需非常注意避免过度牵拉额颞部皮瓣,以防对面神经颞支造成牵拉损伤。
偏好的技术是进行开颅及颧骨、颧弓截骨(使用摆动锯),以获得一个完整的翼点-眶颧联合骨瓣。与常规翼点开颅相比,眶颧开颅的主要优势在于其提供了更有利的自下而上的视角轨迹,仅需轻微抬起额叶即可处理向上延伸至Monro孔水平的肿瘤上极部分。尽管此种颅底入路操作更为费力耗时,但其同样能获得良好的美观效果。
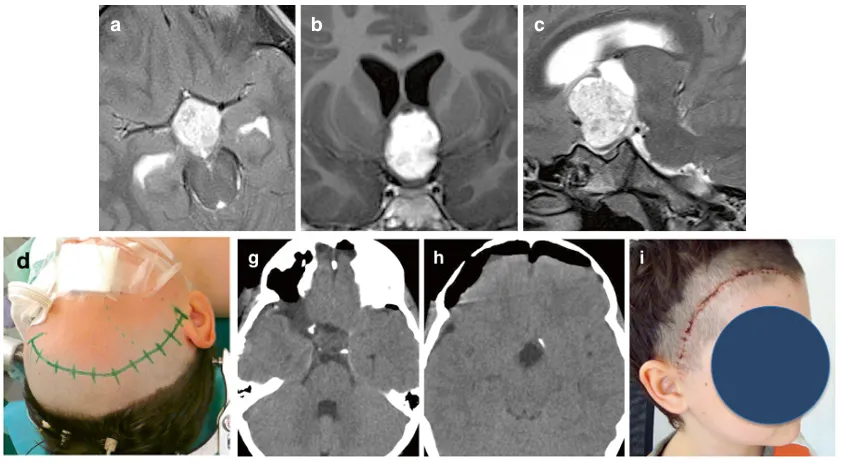
图:一名8岁男性患儿因视路-下丘脑胶质瘤累及第三脑室出现视力受损,采用右侧眶颧开颅入路经终板入路成功实现肿瘤全切。术后早期CT证实全切,美容效果满意。
额底中线开颅联合纵裂入路技术解析
患者取仰卧位,抬高下肢及上半身,头部略向后伸展。皮肤切口标记在发际线后方,除既往手术遗留局部瘢痕者外,通常为双侧对称切口。儿童与青少年或成人患者的区别在于年幼儿童无额窦,这简化了额底中线开颅。
青少年及成人通常有大小不一的额窦,必须在开颅和手术结束关颅时予以考虑。术前CT扫描可清晰显示额窦的大小、形状和范围;术中,在神经导航辅助下确定其上界和外侧界。切开皮肤后,将额部皮瓣翻向下至眶缘。在高位额部区域及沿双侧颞上线切开骨膜,并同样向下翻至眶缘水平。由此获得一个带血管蒂的骨膜瓣,在手术结束时硬脑膜水密缝合后,可用其立即覆盖额窦(额窦颅腔化)。
需注意清除骨瓣上所有残留的额窦黏膜,以防术后形成黏液囊肿。开颅并悬吊硬脑膜后,从外侧向内侧切开硬脑膜,结扎上矢状窦,并切断大脑镰在鸡冠的附着点。仔细离断双侧嗅神经周围的蛛网膜,使其与额叶分离。在逐步分离纵裂内蛛网膜后,即可在不牵动嗅神经的情况下向侧方牵开额叶,从而在整个硬膜内手术过程中保留嗅神经。
如此,获得了对视神经、视交叉及Willis环前部的宽敞暴露,肿瘤前部亦可直接抵达。为暴露第三脑室内肿瘤,从下方的视交叉向上至前连合打开终板。对于有明显侧方延伸的病变,曾离断前交通动脉。此操作允许额外的侧方牵拉和安全的肿瘤切除。
此颅底入路的优势在于可获得下丘脑区域的全景视野,不仅能直线、对称地深入第三脑室,还能抵达脚间池和鞍区。与眶颧技术类似,额底纵裂入路更为费力耗时;尽管如此,其同样能提供良好的美观效果。
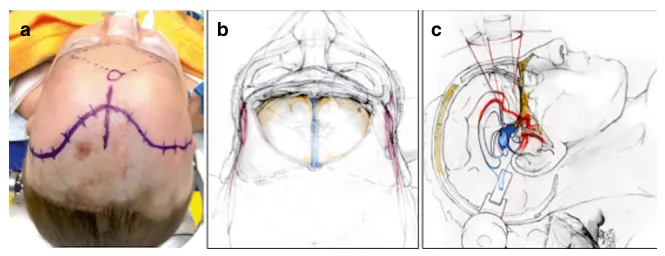
图:额底中线开颅联合纵裂入路示意图,显示患者体位、皮肤切口、开颅范围及经纵裂抵达视交叉-下丘脑区域的路径。

- 所属栏目:胶质瘤
- 如想转载“视路胶质瘤能活多久?27年无复发的背后,手术入路的选择艺术”请务必注明来源和链接。
- 网址:https://www.incsg.com/jiaozhiliu/7645.html
- 更新时间:2026-02-22 13:22:59







