James T . Rutka教授研究:接受颅内记录的儿童睡眠闭环调节
发布时间:2026-03-06 17:54:33 | 阅读:次| 关键词:James T . Rutka教授研究:接受颅内记录的儿童睡眠闭环调节
- [案例]“脑瘤易复发,为何不扩大切除?”——一位32岁女性15年
- [案例]不开颅、不放化疗,脑瘤几乎消失!9岁颅咽管瘤女孩如何
- [案例]跨越千里的生命时速:急性出血期内,脑干海绵状血管瘤
- [案例]令医生直言"棘手"的高级别胶质瘤,两大国际专家协作
- [案例]愿我的小宝贝健康长大!脑瘤开颅术后1年,妈妈为你骄傲
- [案例]6岁脊髓-脑干胶质瘤女孩“劫后重生”:一家人的“开心果
James T. Rutka教授(鲁特卡)曾任世界神经外科学院院长,三十余年来深耕儿童神经外科领域,带领团队在脑瘤分子分型、精准治疗、新药研发及微创治疗等方面持续取得突破,为全球罹患神经外科疑难疾病的儿童带来希望。其团队近期发表了题为《Closed-loop modulation of sleep in children undergoing intracranial recordings》(接受颅内记录的儿童睡眠闭环调节)的研究,以下为该研究的简要概述。

01 关键要点
相位靶向听觉刺激能够增强癫痫患者大脑的慢波睡眠活动。
通过颅内电极记录,探测了参与睡眠调节过程的丘脑皮质网络。
夜间实施刺激可使睡眠期间的发作间期放电减少75%。
经过隔夜刺激后,受试儿童在次日反应抑制任务中的正确率从76%提升至95%。
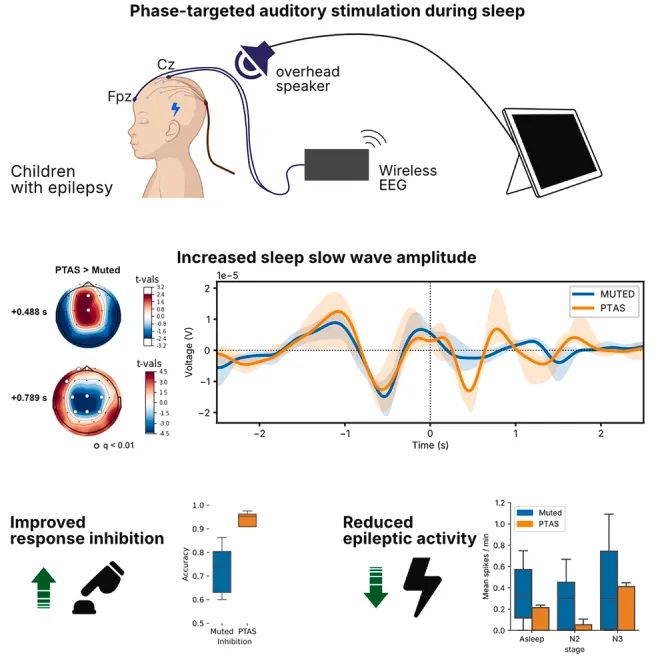
在睡眠期间施加相位靶向听觉刺激,能够增强癫痫儿童的慢波活动,并获得了大规模丘脑皮质网络参与的颅内直接证据。此种非侵入性方法可显著减少睡眠期间的癫痫样放电,同时改善受试者在次日反应抑制任务中的认知表现。
02 研究摘要
癫痫儿童常陷入一种恶性循环:睡眠紊乱会加剧其发作易感性,而癫痫发作本身又会进一步破坏睡眠质量,尤其损害对认知、免疫及代谢功能至关重要的慢波睡眠。本研究提出一种相位靶向听觉刺激系统,该系统在与内源性慢振荡的特定相位同步时施加听觉刺激。在27名同时接受头皮、颅内及丘脑记录的癫痫监测儿童中,通过随机交叉方案,PTAS显著增强了慢波睡眠功率,其中对丘脑、额叶及听觉区域的影响最为显著。刺激同时抑制了发作间期癫痫样放电(尖波计数从每分钟0.4个降至不足0.1个),并改善了一项反应抑制任务的认知表现(正确率从76%提升至95%)。上述结果为闭环听觉刺激能够调节睡眠结构、抑制病理活动并增强认知功能提供了直接的颅内证据。PTAS代表了一种基于生理学原理的非侵入性方法,可用于应对儿科癫痫的神经生理及认知共病问题。
03 研究简介
睡眠在人类健康与福祉的多个层面发挥着基础性作用。其对于身体、代谢及心血管健康,认知功能,情绪健康,生长发育,安全乃至长寿均至关重要。慢性睡眠质量低下、睡眠中断以及睡眠障碍,会显著增加罹患高血压、肥胖、糖尿病及诸多其他不良健康后果的风险。
历史上,优化睡眠的努力主要集中于解决特定睡眠障碍或强调睡眠卫生。近期的技术进步则试图直接增强睡眠的恢复性。闭环相位靶向听觉刺激为直接调节慢波睡眠提供了一条前景广阔的途径,而慢波睡眠是对记忆巩固、代谢调节及免疫功能至关重要的一个睡眠阶段。PTAS通过实时检测慢波振荡,随后在振荡的特定相位传递听觉刺激来实现。此种靶向刺激能够放大慢波活动,进而可能改善认知、代谢健康及其他睡眠依赖功能。值得关注的是,PTAS提供了一种非侵入性且具备潜在可定制性的干预措施,能够靶向睡眠的一个核心恢复性成分。该技术有望改善包括睡眠障碍患者及存在睡眠相关认知功能损害者在内的多种人群的睡眠质量与觉醒功能。
癫痫儿童是需要睡眠靶向干预的重要群体。充足的睡眠对于控制癫痫发作至关重要,部分类型的癫痫仅通过改善睡眠即可获得良好反应。此外,睡眠质量显著影响认知功能,而认知功能是癫痫患者生活质量的关键维度。同时,该人群的颅内记录为阐明PTAS及睡眠过程背后基于源的神经机制提供了独特机会。
在本研究中,我们利用癫痫儿童皮层及皮层下区域(包括丘脑)的同步头皮与颅内脑电图记录,描述了睡眠期间头皮及颅内对听觉刺激的反应,并将其称为夜间听觉诱发电位。随后,我们系统性地描述了在睡眠慢振荡不同阶段诱发nAEP的差异效应,并确定了一个能够稳健增强睡眠慢振荡的相位靶点。我们利用专为癫痫患者PTAS实施困难而开发的闭环设备,在癫痫监测单元内开展为期多天的随机、平衡实验,通过上升相位靶刺激,探究PTAS对发作间期癫痫样放电及认知功能的影响。此项工作填补了我们在睡眠期间听觉刺激生理机制、通路以及PTAS对癫痫儿童影响方面的关键认知空白。
04 研究方法
我们开发了一套系统(参见图1A),用于在儿科癫痫监测单元这一本质动态且复杂的环境内实施PTAS。我们的系统采用小波卷积方法(参见图1B)进行相位跟踪,旨在最小化癫痫样事件对慢波睡眠检测的混杂效应,同时优化闭环反馈时间以改善相位定位精度。相较于常用的阶段定向方法,我们的方法在癫痫脑电图处理中展现出显著优势。
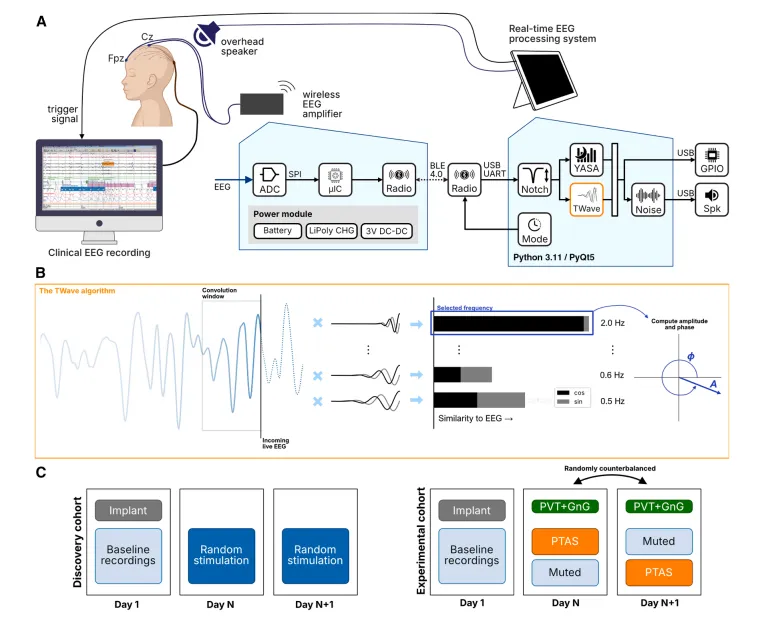
图1.一个基于TWave算法的儿童癫痫PTAS系统及实验设计概述。
(A和B)我们闭环阶段目标听觉刺激系统的示意概述,包括无线脑电放大器、床边计算机及处理软件、用于听觉刺激的床边扬声器,以及用于锁定时间的临床脑电记录系统的触发接口。ADC,模拟/数字转换器;μIC,微控制器;锂聚合物电池充电器LiPoly CHG;直流-直流,直流转直流电压调节器;SPI,串行外设接口总线;BLE,蓝牙低功耗;UART,通用异步接收/发射机;通用输入输出(GPIO);Spk,扬声器。
(B) TWav算法的示意概述:接收的实时脑电图与一组小波进行卷积,以估计频率、幅度和相位,并用于推算即将到来振荡周期中目标相位的时间。
(C)发现组和实验组实验块概述。发现组在一晚或多晚接受随机刺激。实验队列接受随机平衡的PTAS(刺激)和静音(抑制刺激)块,随后每日进行基于计算机的神经认知评估,包括PVT和Go/NoGo任务(GnG)。
研究设计和队列
为验证听觉刺激的可行性并优化刺激参数,我们首先在15名接受随机定时刺激的儿童(男性占比53%,年龄范围8-16岁)中,描述了在睡眠慢波不同相位施加听觉刺激对睡眠电生理学的影响。随后,我们招募了另一个独立的12名儿童队列(男性占比42%,年龄范围9-18岁),使其在一个随机、平衡的区组设计实验中接受PTAS。在所有儿童中,我们利用植入电极(图2D;平均每位参与者140个电极触点,范围70-196)记录了连续脑电图,并同步进行立体定向脑电图记录,从而以高解剖精度和毫秒级时间尺度对大脑区域进行采样。所有儿童均表现出正常的总体睡眠结构(图2A),平均每晚分别有53%、24.5%和18.5%的时间处于N2期、N3期及快速眼动睡眠期,平均睡眠时长为8小时(图2C)。刺激并未显著改变两个队列中各睡眠阶段的时长。平均尖波指数(即睡眠期间观察到发作间期放电的时间比例)为9.5%,且在队列间无显著差异(图1B)。
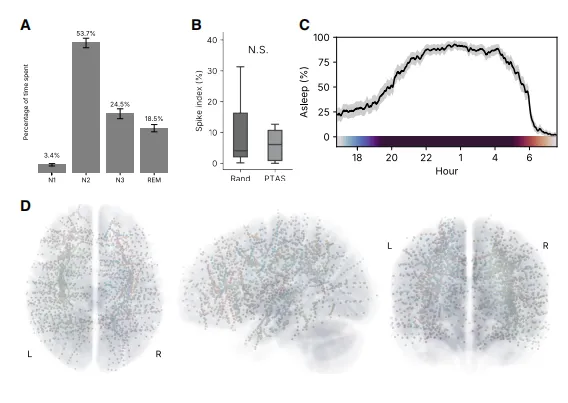
图2.聚合睡眠和尖波指标及电极覆盖图
(A) 所有招募参与者的睡眠结构(各阶段时间占比以平均值±标准误表示)。
(B) Discovery 和 Experimental 队列的尖波指数(尖波指数箱线图表示中位数、四分位距及±1.5倍IQR)。
(C) 一天中聚合的睡眠可能性显示正常的平均睡眠开始和醒来时间(平均百分比±标准误)。
(D) 所有受试者(N=27)植入电极位置的聚合图,已配准到蒙特利尔神经学研究所标准空间。
05 研究结果
(1)夜间听觉诱发电位
我们首要目标是利用同步的头皮与颅内记录,来表征夜间听觉诱发电位的颅内来源及其演变过程。在Discovery队列(接受随机刺激)中,通过计算刺激锁定的平均时间序列,我们在15名受试儿童中的9名成功诱发出nAEP的个体中识别出了该电位。在其余未能检测到nAEP的儿童中,我们发现音频头带在夜间发生了移位或松动。Discovery队列的儿童平均每晚接受284±17次刺激。癫痫儿童nAEP的头皮拓扑图显示其主要集中在中部区域,波形尖锐(图3,左上),这与先前在健康儿童中的报告结果相似。按脑叶解剖结构平均后总结的颅内信号区域时域波形亦展示于图3(左下)。
为表征颅内nAEP在组水平上的空间模式,我们直接对时域数据矩阵(样本×区域)应用了主成分分析。此种分解产生了每个成分的时间不变空间载荷(渲染为脑图)及相应的时间过程(图3,右上),从而捕获了跨区域的协同活动模式,同时降低了数据维度。
第一主成分在其时间过程中显示出一个在450毫秒达到峰值的显著负向波,其空间载荷呈现弥散的前-中央-顶叶内侧拓扑结构,在下颏叶和颞叶区域则观察到与之匹配但极性相反的正电位。第二主成分包含一个在300毫秒出现的正向峰值,随后在顶叶、下颏叶及内侧颏叶区域出现一个在660毫秒的负向峰值。主成分3与C2大致相似,涉及颏叶区域,在297毫秒有一个更早、更尖锐的正峰,随后在450毫秒出现一个负峰。主成分4显示出最早的在200毫秒的峰值,振幅相对较低,在下颏叶、腹侧前扣带回、下顶叶及后扣带回区域呈现出一种看似振荡的形态(图3,右)。
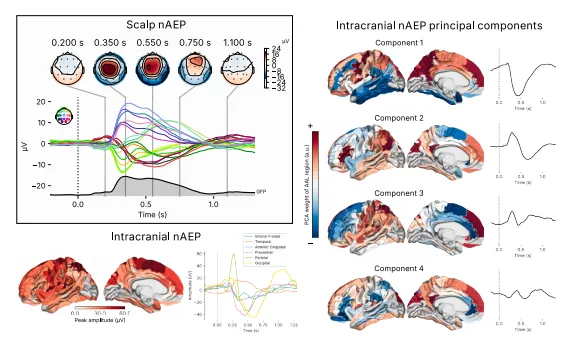
图3.nAEP的头皮波形和时间解析头皮拓扑结构(左图)。来自颅内记录的四大时间锁定nAEP主要组成部分的拓扑和时间序列,均在自动解剖标记v.3(AALv3)区域内进行平均。
(2)上升相位刺激选择性地增强睡眠慢波振荡
为探究振荡功率差异背后的电生理学基础,我们随后分析了刺激相位对睡眠慢振荡差异时间及拓扑演变的影响。基于观察到的相位与慢振荡功率关系(图4A),随机传递的刺激被二分化为上升相位(7π/6到π/6)或下降相位区间。首先,我们观察到Fpz-Cz导联的相位对齐诱发电位(图4B,下图)在上升相位刺激下显著更高。其次,上升相位刺激与跨越中、下颏叶、扣带回、中央前后回、顶叶和颞回的广泛网络的显著更高的颅内慢振荡功率相关(图4C)。第三,我们观察到上升相位刺激促进了典型的慢振荡前-中央拓扑结构的增强(图4B,见0.5-1.0秒)。下降相位刺激则与这种拓扑结构的分裂及慢振荡促进作用的减弱相关。下降相位刺激后,先前在基线期观察到的前-中央拓扑结构不再存在(图4B,顶部在+0.5秒),慢振荡频段的功率较低(图4A),并且头皮电位未出现刺激后增加(图4B,底部)。
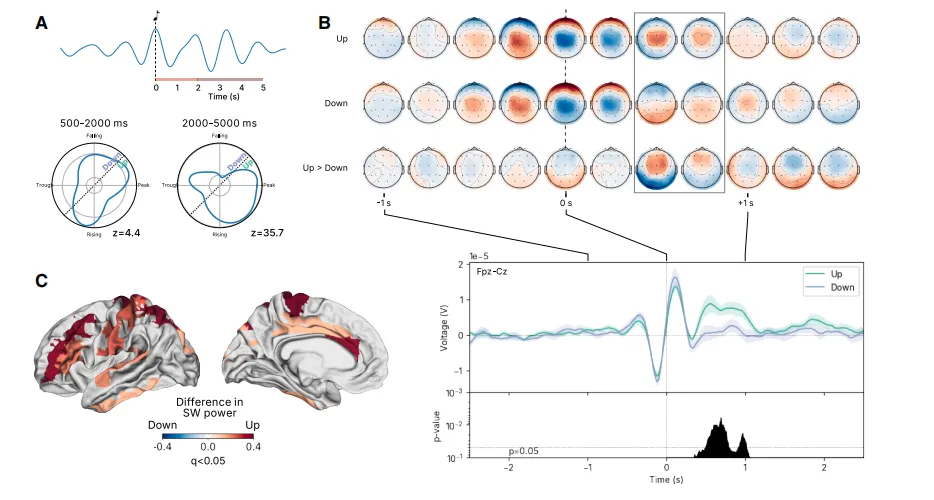
图4.(A) 刺激后短波功率(0.5–2.0 Hz;径向轴)作为刺激时短波相位(角轴)的函数,显示在上升和峰值阶段功率较高。两种分布的瑞利Z(Rz)值表明振幅相位分布存在显著的不均匀性。(B)在刺激的上升和下降阶段,平均刺激锁定时间序列显示,相较之下阶段刺激,上升阶段刺激后刺激后活动显著增加(阴影表示95%自助置信区间[CI])。(C)上相针对性的听觉刺激可提升中额、中部、扣带骨和颞部的超声波功率。
(3)上升相位PTAS增加癫痫儿童的慢波振幅
在Experimental队列中,儿童平均在上升相位PTAS条件下接受319±42次刺激,在静音条件下接受330±36次刺激。与静音条件相比,上升相位PTAS导致Fpz-Cz双极导联的慢波振幅在刺激后高达1.8秒内显著增加(图5A)。在时频分解分析中(图5B),我们发现上升相位PTAS在传递听觉刺激后高达3秒内显著增加了慢振荡功率。
为识别受上升相位PTAS影响的皮质区域,我们计算了PTAS和静音两种条件下整个头皮的诱发反应(图5C-5F)。在上升相位PTAS条件下,我们观察到一个以前-中央为主的诱发反应,它同步持续了几个额外的周期。两种条件下基线区间的睡眠慢振荡在组间无显著差异。在MNE-Python峰值查找功能确定的时间点,我们观察到上升相位PTAS条件下在前-中央区域的慢振荡功率显著增加。
使用解释受试者和夜间随机效应的线性混合效应模型,我们识别了上升相位PTAS的颅内关联,并观察到慢振荡功率增加定位于前扣带回、内侧额上回、Rolandic区和内侧眶额皮质,并且独特地定位于丘脑(图5G)。在8名有丘脑电极的儿童中,上升相位PTAS也在丘脑观察到了显著的诱发反应(图5H),但与我们的头皮记录相反,我们未在丘脑观察到相应的基线(即检测)慢振荡。
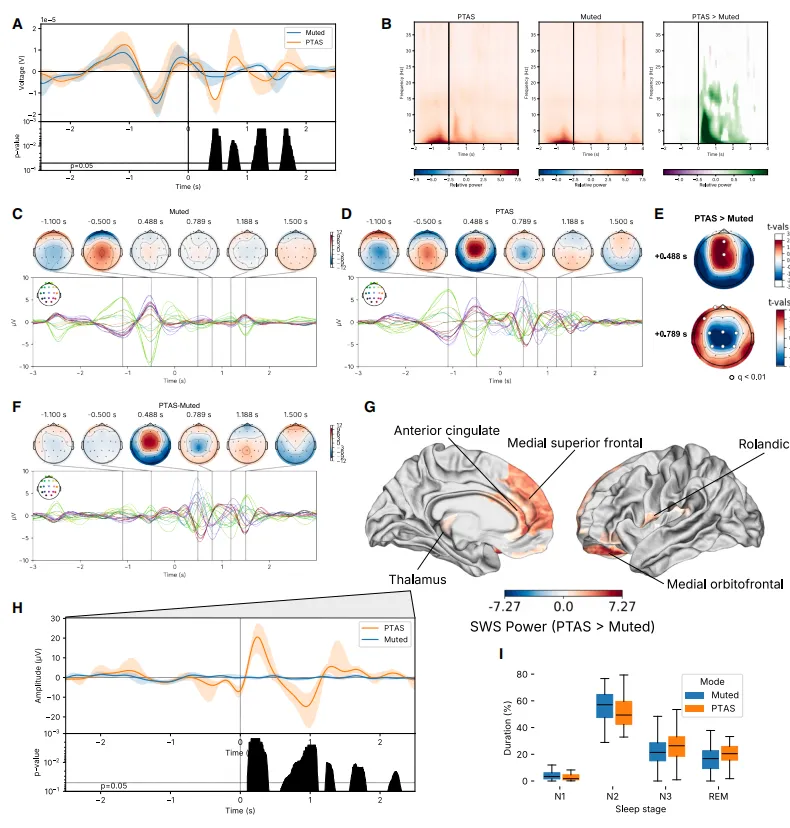
图5.实验队列中,up-PTAS与减弱条件下的平均刺激锁定时间序列显示,Fpz-Cz蒙太奇中SO活性显著增加(A,诱发;B,时间和频率解析分解),其中阴影代表95%的自助置信区间。在静音(C)和上PTAS(D)条件下,头皮时间序列显示,并显示差值(F)。在MNE峰值探测器选定的关键时间点,up-PTAS使广泛的头皮脑电传感器(E, q < 0.01,配对t检验)的SO活动显著增加。同样,在我们的颅内记录中,额中央和颞部区域及丘脑在PTAS(G)下表现出更高的慢振荡能力。在丘脑中,尽管丘脑(H)缺乏刺激前基线SO,但PTAS仍导致强烈的诱发听觉反应,阴影占95%的自助置信区间。PTAS和静化状态的睡眠结构无显著差异(I);箱形图表示中位数、IQR和±1.5 IQR。
(4)上升相位PTAS减少睡眠期间的癫痫样放电
为探究上升相位PTAS对癫痫样活动的影响,我们使用先前建立的自动尖波检测器标记了发作间期放电。随后我们比较了上升相位PTAS和静音条件下的发作间期放电发生率。来自随机平衡的Experimental队列的数据显示,在N2和N3睡眠期间,与停止刺激的区块相比,上升相位PTAS区块中的发作间期放电发生率显著降低(图6C)。在仅考虑颏叶、颞叶、顶叶和枕叶头皮脑电图电极记录的发作间期放电的亚组分析中也观察到了类似的模式(图6E)。为评估发作间期放电的减少是否发生在上升相位PTAS的紧邻时间窗口内,我们进行了发作间期放电可能性相对于刺激的时间分辨分析,发现上升相位PTAS导致刺激后5秒期间尖波可能性显著下降(图6D)。
(5)上升相位PTAS改善抑制控制
鉴于慢波睡眠和PTAS已被证明能改善成人群体的神经认知结局,我们试图评估上升相位PTAS对癫痫儿童的神经认知后遗症。我们使用成熟的Go/NoGo任务(图5J)来评估反应抑制,这是一个对睡眠敏感的认知领域,在癫痫儿童中常受损害。在经历上升相位PTAS的夜晚之后,我们发现与未传递刺激的夜晚相比,反应抑制的正确率显著提高(平均95%对比平均76%;图6F)。
为确保更强的反应抑制结果并非由任务期间的警觉状态驱动,我们还测量了Go/NoGo任务警觉条件以及独立的心理运动警觉任务的表现。我们发现Go/NoGo警觉条件的正确率以及心理运动警觉任务的反应时间或正确率,在有和没有PTAS的夜晚之间没有差异。
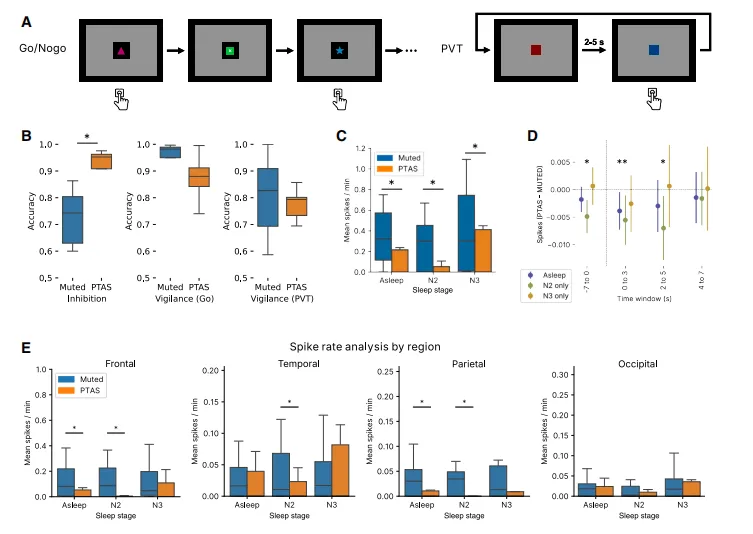
图6.儿童每天接受Go/NoGo和PVT计算机任务的神经认知测试(A)。在PTAS之后,我们观察到反应抑制方面神经认知表现显著提升,指标为Go/NoGo任务的准确率(∗p = 0.002线性混合效应[LME]在B组)。以警觉状态和PVT为指标的警觉性不显著。我们观察到PTAS整体峰值率显著下降(N2:p < 0.001 LME,N3:p = 0.007 LME;C)以及刺激后立即的尖峰率显著下降(D;∗p < 0.05 LME)。峰值率的下降在各地区基本一致(E;∗q < 0.05 LME)。箱形图表示中位数、IQR和±1.5 IQR。条形图显示了SEM±均值。点阵图(D)显示LME估计值及95%置信区间。
06 讨论
睡眠对健康至关重要,而癫痫儿童尤其容易受到睡眠碎片化对发作控制和认知的影响。睡眠调节,即睡眠慢振荡调节,最近已成为一种增强睡眠恢复性特性的非侵入性策略。尽管睡眠期间的闭环听觉刺激是一个活跃的研究领域,但神经调节的颅内效应以及PTAS在癫痫儿童中的作用尚未得到充分描述。在本报告中,我们介绍了一种用于跟踪和估计癫痫儿童脑电图中振荡相位的系统。在具有同步头皮和颅内脑电图的Discovery队列中,我们表明上升相位PTAS与下降相位PTAS相比,在头皮记录以及涉及听觉、额叶、中央和扣带回路的丘脑皮质网络中,能更大程度地增强睡眠慢振荡。丘脑参与的结果通过丘脑靶向电极得到了独特的证实。然后,我们设计了一项随机、平衡的实验,向我们的Experimental队列施加上升相位PTAS和静音(停止)刺激区块。我们报告了慢振荡的增强,同时伴随着发作间期放电的减少和睡眠相关认知领域——抑制控制的改善。当前的发现为PTAS的颅内机制以及癫痫中睡眠调节的途径提供了详细的见解。
07 研究局限性
由于在复杂动态的临床环境中纳入儿科人群,我们解释这些发现的能力存在固有的局限性。第一,本研究在癫痫监测单元进行,与典型的受控睡眠实验室环境不同。我们的参与者队列确实在其人口统计学、癫痫状况和颅内监测手术计划方面存在变异性。第二,我们的数据无法描述长期PTAS对发作活动或神经认知的影响。最后,虽然所有睡眠阶段都很重要,但我们的实验仅在非快速眼动睡眠期间施加PTAS。
因此,我们的发现和这些局限性指出了几个进一步研究的方向,值得注意的是,一项更长持续时间的实验,测试PTAS在数周至数月内的效果,这在立体定向脑电图电极下是不切实际的。未来的研究还可以在颅内层面针对慢振荡开展刺激,靶向参与睡眠调控的皮层及皮层下结构,包括丘脑和前岛叶;或者靶向与患者个体化癫痫致痫网络相关的脑区。

- 所属栏目:神外资讯
- 如想转载“James T . Rutka教授研究:接受颅内记录的儿童睡眠闭环调节”请务必注明来源和链接。
- 网址:https://www.incsg.com/shenwaizixun/7724.html
- 更新时间:2026-03-06 17:44:21







