对1000余例髓母细胞瘤基因组进行亚组特异性结构变异分析
发布时间:2026-03-07 21:37:02 | 阅读:次| 关键词:对1000余例髓母细胞瘤基因组进行亚组特异性结构变异分析
- [案例]7年3次脑干出血,38岁男子勇闯手术关,肿瘤全切重获新生
- [案例]头晕、平衡变差别硬抗!可能是脑瘤生长的信号!
- [案例]半年内脑干胶质瘤体积翻倍,术后9天他迫不及待:我想回
- [案例]7岁男孩一颗巨大脑瘤贯穿脑干:从走路跌倒到3公里“小飞
- [案例]9岁男孩罹患“较大视神经胶质瘤“,失明危机下,INC巴教
- [案例]颅咽管瘤哪里逃?施罗德教授为7岁小勇士击败脑中“怪兽
INC国际儿童脑瘤领域权威专家、世界小儿神经系统专业杂志《Child's Nervous System》现任主编Concezio Di Rocco教授,近期发表了一项题为《Subgroup specific structural variation across 1,000 medulloblastoma genomes》(对1000余例髓母细胞瘤基因组进行亚组特异性结构变异分析)的研究。以下为该研究内容的简要概述。

01 摘要
髓母细胞瘤属于最常见的恶性儿童脑肿瘤,当前临床治疗主要采用非特异性细胞毒性疗法,具体涵盖手术切除、全脑放疗以及强化化疗等方案。鉴于髓母细胞瘤呈现出显著的肿瘤间异质性,其至少包含四种不同的分子亚型,先前由于样本量有限,识别治疗靶点的尝试在统计效能上存在不足。本研究报告了1087例独特髓母细胞瘤病例中的体细胞拷贝数变异情况。SCNAs在髓母细胞瘤中较为常见,且主要表现出亚组富集特性。最常见的局灶性拷贝数增加区域为帕金森病基因SNCAIP的串联重复,该重复现象严格局限于Group 4a亚组。涉及PVT1的复发性易位,包括通过染色体碎裂过程产生的PVT1-MYC及PVT1-NDRG1融合,则局限于Group 3亚组。诸多可靶向的SCNAs,例如Group 3中靶向TGFβ信号通路的复发性事件,以及Group 4中靶向NF-κB信号通路的事件,为未来开展合理的靶向治疗指明了潜在方向。
脑肿瘤是儿童肿瘤相关死亡的首要原因,而髓母细胞瘤则是最常见的恶性儿童脑肿瘤。现行的髓母细胞瘤疗法包括手术切除、全脑及脊髓放疗、强化化疗,并辅以骨髓移植,其五年生存率约为60-70%。然而,幸存者常因这些非特异性细胞毒性疗法对发育中大脑的影响,而遗留严重的神经、智力及身体功能障碍。
现有证据表明,髓母细胞瘤实际上包含多个在分子层面存在差异的实体,其临床与遗传学差异可能需要采取单独的治疗策略。目前已明确髓母细胞瘤存在四个主要亚组:WNT、SHH、Group 3及Group 4,且有初步证据显示这些亚组内部存在具有临床意义的分支。目前,基于遗传学的合理靶向疗法尚未应用于髓母细胞瘤的治疗,尽管Sonic Hedgehog通路蛋白Smoothened的抑制剂已显示出早期应用前景。针对WNT、Group 3及Group 4肿瘤的可操作靶点尚未确定。对22个髓母细胞瘤外显子组进行的桑格测序显示,平均每个肿瘤仅存在8个SNV。部分SNV具有亚组限制性(如PTCH1、CTNNB1),而其他则跨亚组发生(如TP53、MLL2)。我们推测,观察到的肿瘤间异质性可能导致先前识别合理治疗靶点的尝试在统计效能上存在不足。
髓母细胞瘤高级基因组学国际联盟(MAGIC)汇集了来自全球46个城市的科学家与医生,收集了超过1200例髓母细胞瘤样本,并利用SNP芯片进行了研究(n=1239;见图1a)。通过定制的nanoString-based RNA检测法,确定了827例病例的髓母细胞瘤亚组归属。在不同亚组中观察到了各异的广泛细胞遗传学获得与缺失模式(见图1b)。运用GISTIC2对整个队列进行分析以识别显著的“驱动”事件,共确定了62个复发性SCNA区域(见图1c);按亚组进行分析则提升了检测灵敏度,从而识别出110个候选“驱动”SCNAs,其中绝大多数表现出亚组富集特性(见图1c-e)。
研究确定了28个复发性高水平扩增区域(拷贝数≥5)(见图1d)。最普遍的扩增影响MYC家族成员,其中MYCN扩增主要见于SHH及Group 4亚组,MYC扩增主要见于Group 3亚组,而MYCL1扩增则见于SHH髓母细胞瘤。多个基因/区域仅在SHH亚组中发生扩增,包括GLI2、MYCL1、PPM1D、YAP1及MDM4(见图1d)。
复发性纯合缺失极为罕见,在1087个肿瘤中仅检测到15例(见图1e)。靶向已知肿瘤抑制因子PTEN、PTCH1及CDKN2A/B的纯合缺失最为常见,且均在SHH病例中富集(见图1e)。新发现的纯合缺失包括KDM6A,这是一种在Group 4亚组中发生缺失的组蛋白-赖氨酸去甲基化酶。使用定制的nanoString CodeSet在192个MAGIC病例中对24个显著的获得区域进行了验证,验证率达到90.9%。我们的结论是,SCNAs在髓母细胞瘤中较为常见,且主要表现出亚组富集特性。
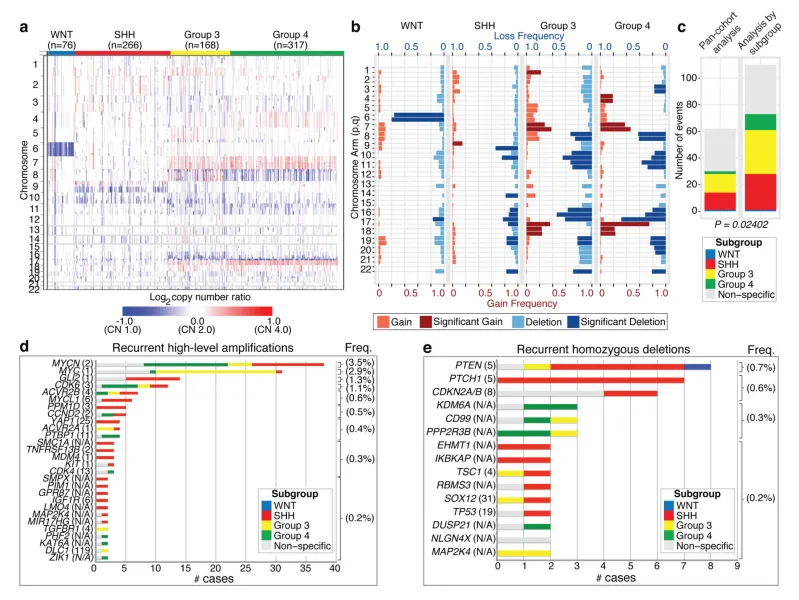
图1.髓母细胞瘤亚组的基因组异质性。a,髓母细胞瘤基因组按亚群分类。b,髓母细胞瘤亚组中广泛细胞遗传事件的频率和显著性(q值≤0.1)。c,通过泛队列或亚组特异性分析GISTIC2识别出显著的局灶性SCNA区域。d, e,髓质母细胞瘤中反复出现高水平扩增(d;分节CN≥5)和纯合缺失(e;分节CN≤0.7)。在疑似驱动基因后,映射到GISTIC2峰值区域的基因数量(如适用)以括号标示,每个事件的频率也显示在其中。
02 研究结果
(1)髓母细胞瘤亚组特异性SCNAs解析
WNT髓母细胞瘤基因组缺乏复发性局灶SCNA区域,未发现显著的缺失区域,仅有一小部分局灶性获得的频率与非WNT肿瘤相当。CTNNB1突变筛查证实,在63/71例(88.7%)WNT肿瘤中存在典型的外显子3突变,而在58/76例(76.3%)中检测到6号染色体单体性。有4例WNT肿瘤(4/71;5.6%)既无CTNNB1突变也无6号染色体单体性,但仍保持了典型的WNT表达特征。考虑到我们队列的规模及平台的分辨率,我们得出结论:对于WNT髓母细胞瘤,不存在频繁的、可靶向的SCNAs。
SHH肿瘤表现出多个显著的局灶性SCNAs(见图2a)。SHH富集/限制性的SCNAs包括GLI2的扩增及PTCH1的缺失(见图2a, e, f)。MYCN和CCND2是SHH亚组中最常扩增的基因之一,但在非SHH病例中也发生了改变。在SHH肿瘤中上调的基因(即SHH特征基因)在SHH肿瘤中发生局灶性扩增的基因中显著富集(P=0.001-0.02,置换检验)。SHH特征基因的复发性扩增具有临床意义,因为下游转录靶点的扩增可能介导对上游SHH通路抑制剂的耐药性。
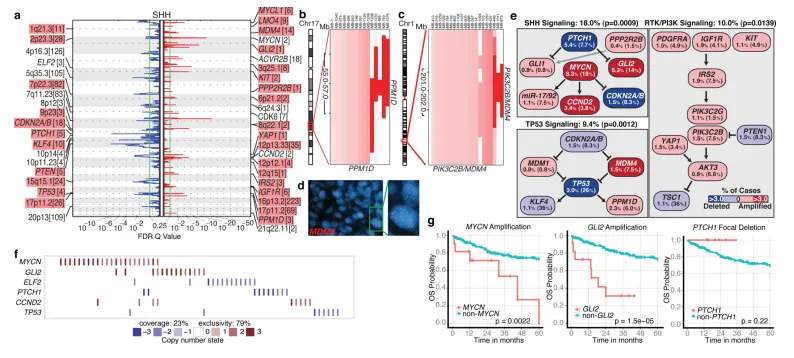
图2.基因组改变影响SHH髓质母细胞瘤的核心信号通路。a,SHH中观察到的扩增(红色)和缺失(蓝色)的显著性图GISTIC2。每个重要区域的基因数量以括号标注,富含SHH的区域以红色阴影标示。b,c,PPM1D(b)和PIK3C2B/MDM4(c)的反复扩增仅限于SHH。d,FISH对MDM4扩增的验证。e,SHH信号、TP53信号和RTK/PI3K信号代表了SHH基因组靶向的核心通路。P值表示SHH与非SHH病例中相应通路的流行率(Fisher精确检验)。列出了焦点和广义(括号内)SCNA的频率。f,SHH中局灶性SCNA的互斥性分析。g,SCNAs影响SHH(对数秩检验)中MYCN、GLI2或PTCH1的临床意义。
新发现的、SHH富集的SCNAs包括TP53信号通路的组成部分,例如MDM4和PPM1D的扩增,以及TP53的局灶性缺失(见图2a-e)。可靶向的事件,包括IGF信号传导基因IGF1R和IRS2的扩增,PI3K基因PIK3C2G和PIK3C2B的扩增,以及PTEN的缺失,均局限于SHH肿瘤(见图2a,c,e)。重要的是,影响SHH通路基因的局灶事件在很大程度上表现出互斥性且具有预后意义(见图2f, g)。在SHH髓母细胞瘤中发现的许多复发性、可靶向的SCNAs(如IGF1R、KIT、MDM4、PDGFRA、PIK3C2G、PIK2C2B和PTEN)已通过小分子靶向用于治疗其他恶性肿瘤,这可能为SHH患者亚组快速转化应用靶向治疗提供可能。此处鉴定的新SHH靶点是与Smoothened抑制剂联合治疗以实现协同疗法、避免在人类和小鼠中遇到的耐药性的优秀候选者。
Group 3和Group 4髓母细胞瘤的命名反映了对其遗传基础认知的不足,且尚未确定合理治疗的靶点。MYC扩增子主要局限于Group 3,而MYCN扩增子则在Group 4和SHH肿瘤中可见(见图1d)。事实上,MYC和MYCN基因座分别构成了在Group 3和Group 4中观察到的最显著的扩增区域(见图3a,b)。Group 3的MYC扩增子与那些影响已知的髓母细胞瘤癌基因OTX2的扩增子是互斥的,并且具有高度预后性。II型激活素受体ACVR2A和ACVR2B以及家族成员TGFBR1在Group 3肿瘤中高度扩增,表明TGFβ信号传导失调是Group 3的驱动事件(见图3c-e)。Group 3富集的髓母细胞瘤癌基因OTX2是发育中神经系统TGFβ信号传导的突出靶点,而TGFβ通路抑制剂CD109、FKBP1A和SNX6在Group 3中复发性缺失(见图3a, d)。TGFβ通路基因中的SCNAs在Group 3中高度富集(P=5.37E-05,Fisher精确检验),并且在至少20.2%的病例中发现,表明TGFβ信号传导代表了这一预后不良亚组的第一个合理靶点(见图3d)。类似地,在Group 4中鉴定出影响NF-κB通路调节因子(包括NFKBIA和USP4)的新缺失,提出NF-κB信号传导可能代表一个合理的Group 4治疗靶点。
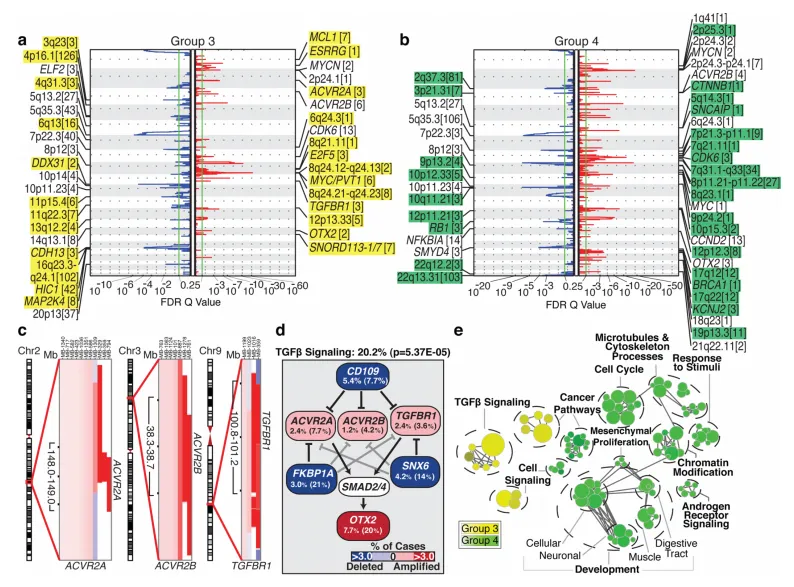
图3.第3组和第4组髓母细胞瘤的基因组图谱。a, b,GISTIC2图显示了第3组(a)和第4组(b)中显著的SCNAs,亚组富集区域分别以黄色和绿色阴影表示。c,针对第三组II型(ACVR2A和ACVR2B)和I型(TGFBR1)活化蛋白受体的反复扩增。d,影响第3组TGFβ通路的复发SCNAs(P=5.73E-05,Fisher精确检验)。列出了焦点和广义(括号内)SCNA的频率。e,受SCNA影响的基因集富集图,分别为第3组与第四组。
对Group 3和Group 4的SCNAs进行网络分析,阐明了每个亚组中富集的不同通路。只有TGFβ信号传导是Group 3独有的(见图3e)。相比之下,细胞周期控制、染色质修饰和神经元发育都是Group 4富集的。总而言之,Group 3患者预后不良、缺乏已发表的合理治疗靶点以及先前在其他疾病中靶向TGFβ信号传导的事实表明,TGFβ可能代表Group 3合理治疗的一个有吸引力的靶点。
(2)SNCAIP串联重复在Group 4中常见
尽管Group 4是最普遍的髓母细胞瘤亚组,但其发病机制仍知之甚少。在Group 4中观察到的最常见的SCNA(33/317;10.4%)是chr5q23.2上靶向单个基因SNCAIP(α-突触核蛋白相互作用蛋白)的复发性单拷贝获得区域(见图4a)。SNCAIP编码SYNPHILIN-1,它与α-突触核蛋白结合,促进帕金森病患者大脑中路易体的形成。此外,在帕金森病家族中已描述过罕见的SNCAIP种系突变。大片段配对末端全基因组测序(WGS)表明,SNCAIP拷贝数增加源于截短的SNCAIP(缺乏非编码外显子)的串联重复,插入到种系SNCAIP等位基因的端粒侧(见图4b, c)。患者匹配的种系材料的SNP6分析证实SNCAIP重复是体细胞性的,随后对选定的Group 4病例(n=5)进行全转录组测序(RNASeq)证实SNCAIP是重复区域中唯一表达的基因。对3131个原发肿瘤和947个癌细胞系(共4078例)已发表的拷贝数谱进行分析,仅发现4例存在明显的SNCAIP重复,所有这些病例都被推断为Group 4髓母细胞瘤(数据未显示)。我们得出结论:SNCAIP重复是高度特异于Group 4髓母细胞瘤的体细胞事件。
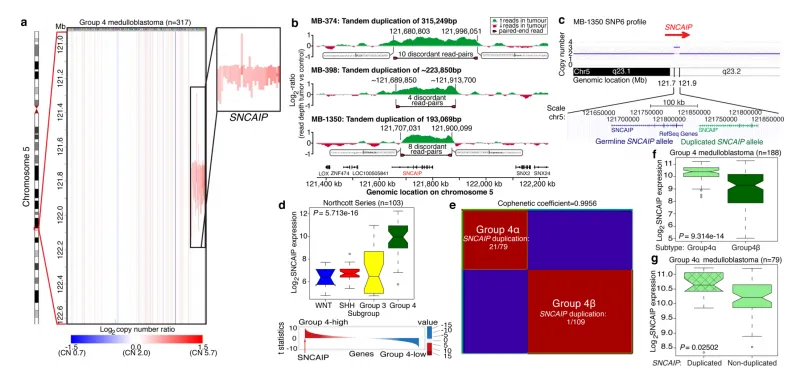
图4.SNCAIP的串联复制定义了第4组的一个新亚型。a,SNCAIP在第4组中高度复发、局灶性、单拷贝增益。b,配对端映射验证了第4组SNCAIP的重复串联重复。c,SNCAIP串联复制的示意图。 d,SNCAIP是第4组特征基因。上方面板。SNCAIP在103例原发性髓母细胞瘤的亚组表达。下面板。SNCAIP在第4组高表达基因中排名前1%(排名=39/16,758)。e,NMF共识聚类188个表达谱的第4组,支持两个转录上不同的亚型,分别命名为4α和4β(表系数=0.9956)。21/22个SNCAIP重复病例属于4α组(P=3.12E-08,Fisher精确检验)。f,SNCAIP在4α组与4β组的表达显著升高(P=9.31E-14,Mann-Whitney检验)。g,4α组携带SNCAIP重复的病例SNCAIP表达增加约1.5倍。
对499个已发表的髓母细胞瘤表达谱的重新分析证实,SNCAIP是Group 4特征基因中上调最显著的基因之一(见图4d)。对188个Group 4肿瘤进行表达芯片分析,然后进行共识非负矩阵分解(NMF)聚类,划分出两个Group 4亚型(4α和4β;见图4e)。引人注目的是,21/22例SNCAIP重复病例属于Group 4α(P=3.12E-08, Fisher精确检验)。SNCAIP在Group 4α中的表达高于4β(见图4f),并且具有串联重复的4α样本显示表达增加约1.5倍,与基因剂量一致(见图4g)。Group 4α与4β相比表现出相对平衡的基因组,并且一些4α病例同时含有SNCAIP重复和i17q而无其他SCNAs。重要的是,SNCAIP重复与Group 4中其他显著的SCNAs(包括MYCN和CDK6扩增)是互斥的。
(3)PVT1融合通过Group 3中的染色体碎裂产生
尽管在实体瘤中发现了复发性基因融合,但在髓母细胞瘤中尚未有报道。Group 3肿瘤(n=13)的RNASeq在两个不同的肿瘤(MB-182和MB-586)中鉴定出两个独立的基因融合,均涉及PVT1的5'端——一个在Group 3中经常与MYC共扩增的非编码基因(见图5a, b)。桑格测序证实了MB-182中存在由PVT1的外显子1和3与MYC的编码序列(外显子2和3)融合而成的融合转录本,以及MB-586中涉及PVT1外显子1与NDRG1 3'端融合的融合(见图5a, b)。
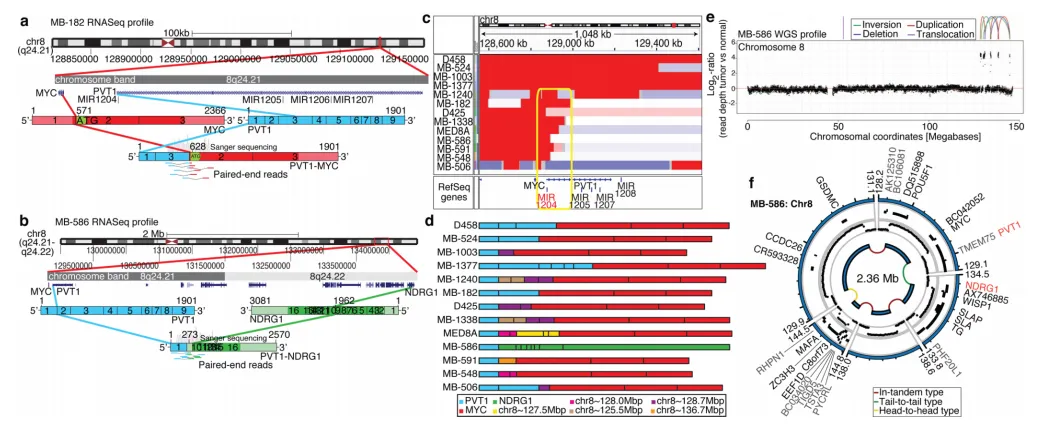
图5.第3组中频繁出现的PVT1-MYC融合基因的鉴定。a, b,RNASeq识别出由PVT1驱动的多个融合转录本,组别为第3组。示意图展示了经验证的PVT1-MYC(b)和PVT1-NDRG1(c)融合基因的结构。c,MYC/PVT1位点热图,显示13例MYC扩增的第3组病例,后证实表现出PVT1基因融合(见d)。黄色框突出显示影响PVT1第一外显子/内含子的共同断点,包括miR-1204。d,第3组中识别的PVT1融合转录本摘要。E, F,WGS确认PVT1融合(+)组3中chr8q24存在复杂的重排模式。
MYC/PVT1基因座的Group 3拷贝数据表明,其他样本可能含有PVT1基因融合(见图5c)。对选定的Group 3病例进行RT-PCR分析证实,至少60%(12/20)的MYC扩增病例存在PVT1-MYC融合(见图5d)。融合转录本包含8q染色体的许多其他部分,多达四个不同的基因组位点映射到一个转录本,这种模式让人联想到染色体碎裂(见图5d)。对四个含有PVT1融合转录本的MYC扩增Group 3样本进行的WGS鉴定出8q染色体上的一系列复杂的基因组重排(见图5e,f)。来自WGS的MB-586(PVT1-NDRG1)的8号染色体拷贝数谱显示,正如RNASeq预测的那样,PVT1和NDRG1在结构上是连接的,并且8q24的几个相邻区域发生了广泛的重排(见图5e, f)。蒙特卡洛模拟表明,这个破碎的8q扩增子是通过染色体碎裂产生的,这是一种在染色体破碎成许多片段的一次灾难性事件后发生错误DNA修复的过程。对我们拷贝数数据集的进一步检查揭示了跨亚组的罕见染色体碎裂示例,只有Group 3中的8号染色体显示出统计学上显著的、区域特异性的染色体碎裂(q=0.0004, FDR校正的Fisher精确检验)。在Group 3肿瘤中,8q染色体碎裂的发生与17p缺失(TP53所在位置)相关(数据未显示),这与最近在髓母细胞瘤中描述的TP53缺失和染色体碎裂的关联一致(P=0.0199, Fisher精确检验)。虽然PVT1基因座被认为是基因组脆性位点,但我们观察到大多数MYC扩增的Group 3肿瘤含有通过符合染色体碎裂的过程产生的PVT1融合。
PVT1是4个miRNA(miR-1204-1207)的非编码宿主基因。先前的研究已暗示miR-1204是一个候选癌基因,与MYC协同增强肿瘤发生。本研究中鉴定的PVT1融合仅涉及PVT1外显子1和miR-1204。重要的是,与融合(-)病例相比,miR-1204(而非相邻的miR-1205和miR-1206)在PVT1-MYC融合(+)的Group 3肿瘤中表达水平更高(P=0.0008, Mann-Whitney检验;见图6a)。为了评估miR-1204的异常表达是否有助于恶性表型,我们在MED8A细胞(一种已确认存在PVT1-MYC融合的Group 3髓母细胞瘤细胞系)中抑制了miR-1204(见图5d)。Antagomir介导的miR-1204 RNAi对MED8A的生长有显著影响(见图6b)。敲低MYC也可实现增殖能力的类似降低。相反,髓母细胞瘤细胞系ONS76既没有MYC扩增,也没有检测到PVT1-MYC融合基因,敲低miR-1204在该细胞系中没有效果(见图6c)。
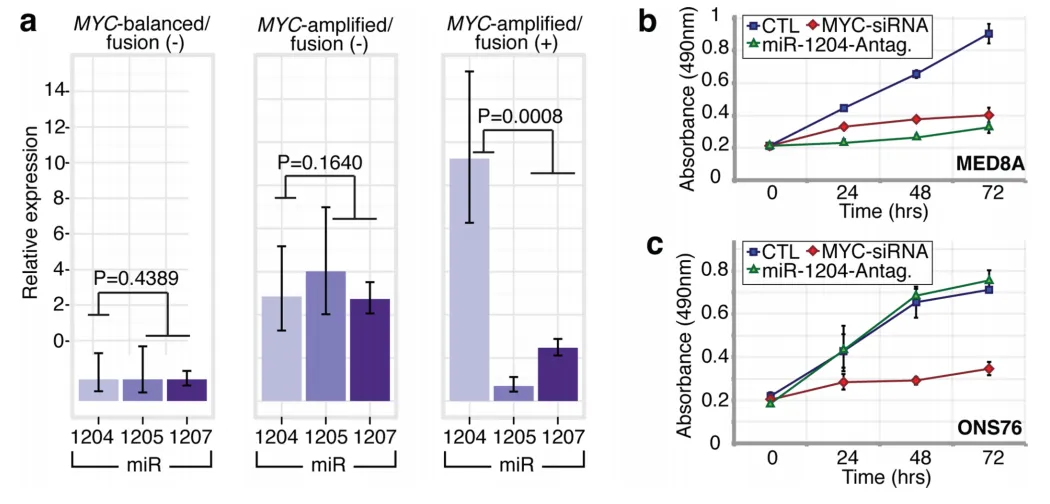
图6.miR-1204与PVT1-MYC融合后继发的MYC功能协同。a,PVT1编码微小RNA的qRT-PCR确认了PVT1-MYC融合(+)组3中miR-1204的上调:MYC平衡/融合(−),n=4;MYC扩增/融合(−),n=6;MYC扩增/融合(+),n=8。误差条代表均值的标准误(SEM),反映样本间的变异性。B,C敲低miR-1204会削弱PVT1-MYC融合细胞(+)MED8A髓质母细胞瘤细胞(b)的增殖能力,但对融合细胞(−)ONS76细胞(c)无影响。误差条表示三重实验的标准差(SD)。
先前已有报道PVT1与多个伙伴形成融合转录本。Group 3肿瘤中最普遍的PVT1-MYC融合形式缺乏MYC的第一个非编码外显子,类似于伯基特淋巴瘤中描述的MYC形式(见图5a, d)。PVT1启动子包含两个非经典E-box,可以被MYC激活。这表明了一个正反馈模型,在PVT1-MYC融合(+)肿瘤中,MYC可以增强其自身从PVT1启动子的表达。事实上,仅在MED8A细胞中敲低MYC就导致MYC和miR-1204的表达均减少,表明MYC可能在髓母细胞瘤细胞中正向调节PVT1(即miR-1204)的表达。
03 讨论
与许多成人上皮恶性肿瘤相比,髓母细胞瘤的SNV很少,而SCNAs似乎很常见。髓母细胞瘤是一种异质性疾病,因此需要大型队列来检测亚组特异性事件。通过在MAGIC中积累超过1200例髓母细胞瘤,我们鉴定出了新的、显著的SCNAs。许多显著的SCNAs是亚组限制性的,高度支持它们在其各自亚组中作为驱动事件的作用。
在神经元细胞中表达SYNPHILIN-1会导致细胞倍增时间减少、caspase-3活化减少、TP53转录活性和mRNA水平降低,以及细胞凋亡减少。SYNPHILIN-1被PARKIN泛素化,PARKIN由遗传性帕金森病基因PARK2编码,是一个候选肿瘤抑制基因。虽然帕金森病患者总体癌症风险降低,但他们患脑肿瘤的发病率可能增加。由于SNCAIP的串联重复是高度复发的、刻板的、亚组限制性的、仅影响单个基因,并且SNCAIP重复的肿瘤几乎没有其他SCNAs,SNCAIP是一个可能的驱动基因,值得作为Group 4α的治疗靶点进行研究。同样,PVT1融合基因是高度复发的、局限于Group 3的、通过染色体碎裂样过程产生的,并且是首次报道的髓母细胞瘤复发性易位。
我们鉴定了许多高度可靶向的、复发的、亚组特异性的SCNAs,这些SCNAs可以作为未来临床试验的基础(例如,SHH中的PI3K信号传导、Group 3中的TGFβ信号传导以及Group 4中的NF-κB信号传导)。通过目前未知的替代遗传和表观遗传事件激活这些通路,可能会增加适合靶向治疗的患者比例。我们还鉴定了一些发生在少数病例中的高度“可成药”事件。MAGIC联盟的合作、全球性方法使我们能够克服这种罕见儿童肿瘤的肿瘤间异质性障碍,并为受影响的儿童识别出相关且可靶向的SCNAs。
04 关于作者


2019年Di Rocco教授和苏附儿医疗团队为孤儿患者进行义诊

Di Rocco教授一生撰写或参与撰写的儿童神经外科部分著作

- 所属栏目:神外资讯
- 如想转载“对1000余例髓母细胞瘤基因组进行亚组特异性结构变异分析”请务必注明来源和链接。
- 网址:https://www.incsg.com/shenwaizixun/7727.html
- 更新时间:2026-03-07 21:27:15







