脑瘤手术风险大,放疗就安全?研究发现儿童放疗不仅可能影响发育,还可能诱发胶质瘤
发布时间:2026-04-18 20:23:05 | 阅读:次| 关键词:脑瘤手术风险大,放疗就安全?研究发现儿童放疗不仅可能影响发育,还可能诱发胶质瘤
- [案例]手脚逐渐增大:垂体腺瘤引发的肢端肥大如何治疗?
- [案例]对抗婴儿痉挛引发的癫痫治疗案例
- [案例]天救自救者,复杂型脑膜瘤患者如何开启“开挂模式”,
- [案例]5年脑出血率30.8%!柳叶刀1620例研究背后,这种脑血管畸形
- [案例]脑膜瘤复发还能治好吗?全面侵袭海绵窦与颈内动脉,第
- [案例]这个病会遗传?3岁女童脑干巨大海绵状血管瘤成功手术后
放射治疗能够提升儿童常见恶性肿瘤的生存率。然而,长期存活的患者可能面临后遗症的困扰,继发性肿瘤即为潜在风险之一。胶质瘤是颅脑或颅脑脊髓区域放疗后较为常见的继发性肿瘤类型,其病理表现多为高级别星形细胞瘤,临床预后通常不佳。
当脑瘤位于手术高风险区域时,放射治疗往往成为一项不得已的选择。一名19岁男性患者,曾在儿童期因髓母细胞瘤接受放疗,后续继发了胶质母细胞瘤;另一名12岁男孩,在胶质瘤放疗后出现了正常脑组织坏死。这两例患者最终均寻求INC巴特朗菲教授进行手术治疗。他们的具体病情如何,下文将进行详细阐述。
这名男孩在7岁时切除了位于第四脑室的髓母细胞瘤,至19岁时又被诊断出小脑胶质母细胞瘤。术后,医生对从右小脑切除的胶质母细胞瘤组织进行了遗传学分析。该例髓母细胞瘤表现出CTNNB1癌基因的热点错义突变、ARID2染色质重塑基因的移码突变、6号染色体单体以及17p缺失合并17q获得,这与等臂染色体17q的特征一致。然而,该胶质母细胞瘤并未包含髓母细胞瘤中观察到的所有突变和细胞遗传学改变。相反,该胶质母细胞瘤含有TP53、STAG2和GATA2的体细胞突变,PDGFRA存在局灶性高水平扩增且扩增等位基因上伴有错义突变,MYCN存在局灶性高水平扩增,以及BCOR存在局灶性纯合性缺失。这些遗传学发现支持了继发性胶质母细胞瘤的诊断,而非髓母细胞瘤的复发。
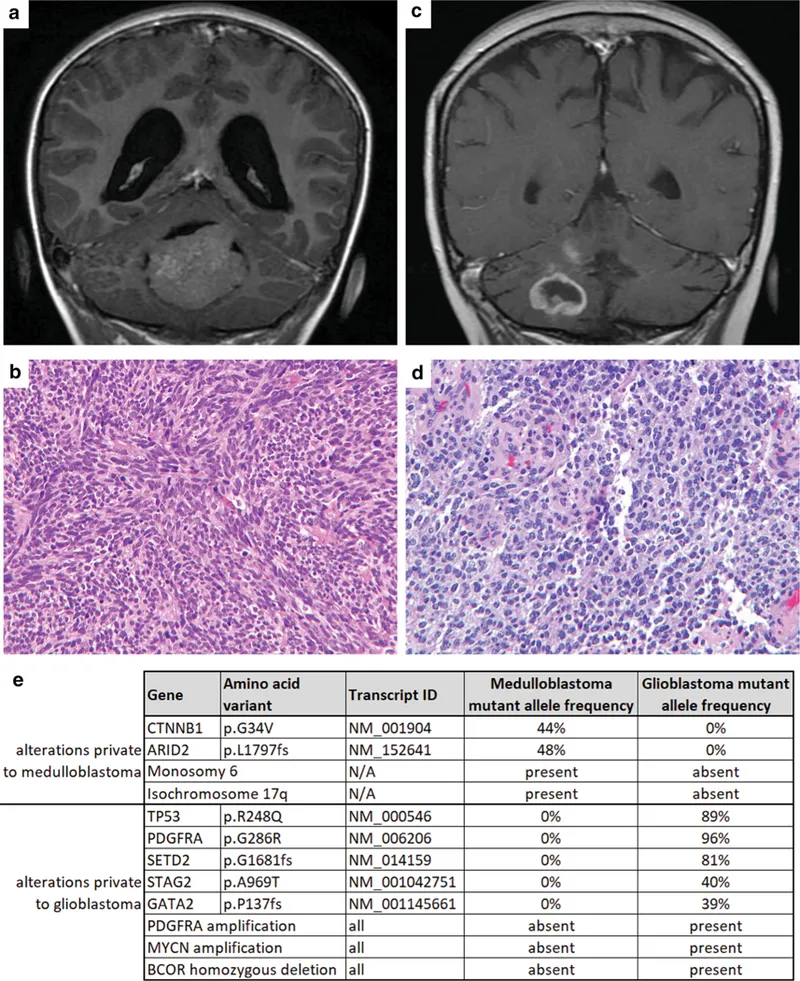
图注:儿童期髓母细胞瘤接受颅脑脊髓放疗后发生的胶质母细胞瘤。a 7岁时的冠状位钆增强T1加权磁共振图像显示第四脑室内髓母细胞瘤。b 组织学显示经典组织学类型的髓母细胞瘤。c 19岁时的冠状位钆增强T1加权磁共振图像显示右小脑周边强化肿块。d 组织学显示伴有微血管增殖的胶质母细胞瘤。e 髓母细胞瘤和辐射相关胶质母细胞瘤靶向测序鉴定的体细胞改变汇总。
这难道是放疗继发的胶质母细胞瘤吗?INC国际神经外科专家针对该男孩在内的12例患者进行了深入研究。这些患者均在放疗后被诊断出胶质瘤,因此对他们进行了遗传学分析,旨在确定其与原发性胶质瘤相比基因组特征的差异。研究发现,这些肿瘤具有高频率的TP53突变、CDK4扩增或CDKN2A纯合性缺失,以及涉及Ras-Raf-MAPK通路基因(如PDGFRA、MET、BRAF和RRAS2)的扩增或重排。值得注意的是,所有肿瘤均不存在IDH1、IDH2、H3F3A、HIST1H3B、HIST1H3C、TERT(包括启动子区)和PTEN的改变,而这些改变是定义儿童和成人弥漫性胶质瘤主要亚型的核心遗传学特征。所有胶质瘤的体细胞突变负荷均非常低(每Mb少于3个体细胞单核苷酸变异或小的插入缺失)。与原发性高级别胶质瘤相比,其中10例高级别胶质瘤表现出明显的非整倍体基因组,其染色体内部拷贝数断点和局灶性扩增/纯合性缺失的数量显著增加,这很可能是γ射线诱导DNA双链断裂的结果。总之,这些发现揭示了放疗后继发性胶质瘤独特的分子发病机制,并确定了一种可能有助于将这些肿瘤与自发性胶质瘤区分开来的基因组特征。

电离辐射的危害性评估
电离辐射应用于癌症治疗已有超过百年的历史,最早可追溯至19世纪末首次使用医疗辐射的Emil Grubbe博士和Victor Despeignes博士。放疗已被证实有助于治愈癌症患者或延长其生存期,尤其对于某些对放疗更为敏感的肿瘤类型,例如淋巴瘤和生殖细胞肿瘤。然而,放疗会伴随急性和晚期副作用。晚期副作用包括因淋巴系统损伤导致的淋巴水肿、因周围神经损伤导致的神经病变、因内皮细胞损伤导致的血管病变、认知功能障碍等等。放疗最严重的晚期后果之一是继发性肿瘤,虽然仅有少数患者会发生,但这是儿童恶性肿瘤长期幸存者的主要死亡原因之一。在脑内,放疗后最常见的继发性肿瘤是脑膜瘤、胶质瘤和肉瘤。此类辐射诱发的胶质瘤通常是与不良预后相关的高级别浸润性星形细胞瘤。
胶质瘤放疗的临床价值探讨
在回答这个问题之前,我们先来看一个真实的临床案例。该案例来源于INC巴特朗菲教授在华实施的示范手术患者。
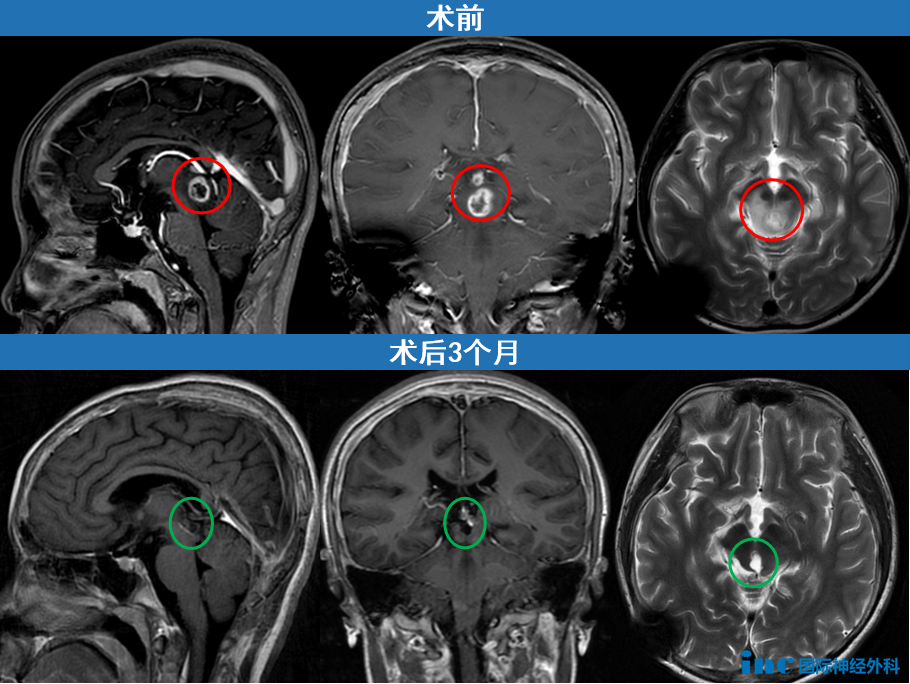
12岁男孩小泰被诊断出脑干中脑肿瘤,当时的接诊医生评估认为手术风险过高,小泰的父母在无奈之下选择了伽马刀治疗。但该治疗并未成功消灭肿瘤,两个多月后,肿瘤仍在持续生长,并且周围正常的脑组织也发生了坏死,其他医生均建议继续观察等待。
此时小泰的父母心急如焚,还要继续等待吗?要知道,“坏死”一旦形成,等待他们的可能只有病情的持续恶化和功能丧失,这不仅关系到原本平静的生活,更直接关系到儿子的生命。在这样的信念支撑下,小泰父母最终决定寻求巴教授进行手术治疗。最终,小泰的肿瘤得到了顺利的全切。手术结束后,小泰无需进入ICU观察,直接转回了普通病房。术后第三天,小泰已经能够正常进食、自主下床活动,各项神经功能恢复良好。如今,他早已回归校园,恢复正常生活。
关于脑胶质瘤的治疗,美国NCCN、欧洲EANO、中国等国际治疗规范指南均明确指出,脑胶质瘤应以手术切除为主要治疗手段,并结合放疗、化疗等综合治疗方法。脑胶质瘤手术治疗的核心原则是在保证安全的前提下,实现最大范围的肿瘤切除。
时间就是生命,面对“死亡恶魔”脑瘤,究竟应该首选手术还是放化疗?这成为摆在疑难脑瘤患者面前的巨大难题。根本问题往往源于对手术风险的恐惧,不敢手术,选择放疗更多是无奈之举。
然而,仅依靠放化疗通常无法使肿瘤完全消失,尤其放化疗在杀伤肿瘤细胞的同时,对正常组织也会造成很大伤害,产生许多化疗副作用,可谓“杀敌一千,自损八百”。随着治疗进程的推进,部分患者会出现急性和远期并发症,影响生存质量,有时这些损害是不可逆的。这对于神经系统仍在发育的婴幼儿而言,影响尤为显著。
此外,一般情况下,对于脑干、神经组织等关键功能区,放射治疗一个人一生通常只能进行一次。一般不能进行二次放射治疗,除非第一次放射治疗剂量不足。因为脑组织对放射治疗有一定的耐受剂量,超过这个剂量会对正常的脑组织造成损害,所以通常不能进行二次放射治疗。
核心分子特征:区别于自发性胶质瘤的独特基因改变谱
回归到上文的研究,研究发现,放疗后继发性胶质瘤缺乏IDH1、IDH2、H3F3A、HIST1H3B、HIST1H3C、TERT(包括启动子区)和PTEN的改变,而这些改变是定义儿童和成人弥漫性胶质瘤主要亚型的遗传学特征。因此,辐射诱发的胶质瘤在分子上似乎不同于成人脑半球发生的IDH突变型弥漫性低级别胶质瘤。此外,辐射诱发的胶质瘤在分子上也似乎不同于儿童和年轻成人中发生的H3 K27M突变型弥漫性中线胶质瘤和脑半球发生的H3 G34R/V突变型弥漫性胶质瘤。与成人脑半球发生的IDH野生型胶质母细胞瘤相比,辐射诱发的胶质瘤缺乏细胞遗传学上表征绝大多数成人自发性IDH野生型胶质母细胞瘤的7号染色体三体和10号染色体单体的组合。此外,它们也缺乏遗传学上表征绝大多数成人自发性IDH野生型胶质母细胞瘤的TERT启动子热点突变和PTEN突变/缺失。
辐射相关高级别胶质瘤(占本队列12例中的10例)在遗传学上具有以下特征:高频率的双等位TP53失活、CDK4扩增或CDKN2A纯合性缺失,以及涉及受体酪氨酸激酶和Ras-Raf-MAPK通路基因的扩增或重排。我们推测,在辐射诱发胶质瘤的发展过程中,TP53突变被早期选择,使得含有大量辐射诱导的染色体重排的肿瘤起始细胞得以存活和扩增。
值得注意的是,TP53突变在辐射诱发的肉瘤中也已被高频发现。与儿童和成人的自发性高级别胶质瘤相似,辐射相关高级别胶质瘤也经常有细胞周期调控基因的破坏。此外,它们也常见受体酪氨酸激酶基因和Ras-Raf-MAPK通路基因的激活。然而,与成人脑半球的IDH野生型胶质母细胞瘤相比,辐射相关高级别胶质瘤很少发生EGFR扩增或突变,而是更常表现为PDGFRA或MET的扩增或突变。与儿童高级别胶质瘤和成人IDH野生型胶质母细胞瘤相比,辐射相关高级别胶质瘤很少发生NF1失活,而是更常表现为BRAF重排或RRAS2局灶性高水平扩增,而后者在已知的任何自发性胶质瘤亚型中均不常发生。这些发现凸显了针对这些通路的靶向治疗的潜在可能性,特别是针对激活的PDGFRA、MET或MEK的激酶抑制剂。
独特的基因组特征:源于DNA双链断裂的结构变异模式
与自发性高级别胶质瘤相比,研究还发现了放疗后继发性高级别胶质瘤独特的基因组特征。这包括每个基因组中染色体内部拷贝数断点的数量、含有多个染色体内部拷贝数断点的染色体数量以及局灶性扩增/纯合性缺失显著增加。大量的染色体内部拷贝数断点分布在基因组的多个染色体上,并不局限于发生染色体碎裂的一两条染色体,而在自发性IDH野生型胶质母细胞瘤中,7号和9号染色体有时会发生染色体碎裂,这可能是导致EGFR扩增和CDKN2A纯合性缺失的机制。因此,除了每个基因组中染色体内部拷贝数断点总数增加外,数个染色体存在增加的染色体内部拷贝数断点,为区分辐射相关胶质瘤和自发性胶质瘤提供了额外的特异性。此外,我们发现辐射相关胶质瘤的体细胞单核苷酸变异负荷较低,这与绝大多数自发性胶质瘤相似。这些发现有助于我们理解电离辐射导致继发性恶性肿瘤的潜在机制。这表明,在治疗原发恶性肿瘤时,电离辐射导致肿瘤起始细胞发生DNA双链断裂,这些细胞经过一段不等的休眠期后,很可能在获得胶质瘤发生所需的额外遗传学改变后,发生克隆性扩增。这些辐射诱导的双链断裂产生了一种独特的基因组特征,将这些肿瘤与自发性胶质瘤区分开来,并且很可能是导致辐射诱发胶质瘤特征性的致癌基因扩增、肿瘤抑制基因纯合性缺失和致癌基因重排的原因。这一假说得到了一个辐射诱发胶质瘤小鼠模型的支持,该模型中,Cdkn2a缺失小鼠经γ射线照射后产生了经常伴有Met扩增的胶质母细胞瘤。
研究意义总结
总之,该项研究明确了儿童恶性肿瘤放疗后继发性胶质瘤的遗传图谱,并展示了一种独特的基因组特征,可将这些肿瘤与其自发性对应肿瘤区分开来。这些发现对儿童癌症的长期幸存者具有重要的诊断和治疗意义。

- 所属栏目:脑瘤治疗
- 如想转载“脑瘤手术风险大,放疗就安全?研究发现儿童放疗不仅可能影响发育,还可能诱发胶质瘤”请务必注明来源和链接。
- 网址:https://www.incsg.com/naoliu/zhiliao/8066.html
- 更新时间:2026-04-18 20:18:23







