儿童有必要做全套分子检测吗?它如何影响各类脑瘤的预后?
发布时间:2026-05-09 10:16:37 | 阅读:次| 关键词:儿童有必要做全套分子检测吗?它如何影响各类脑瘤的预后?
- [案例]钢琴家患丘脑胶质瘤,出现手指细致功能障碍,美妙乐章
- [案例]曾患脑干肿瘤,开颅手术后1个月回归校园,拿下“三好学
- [案例]INC巴教授“禁区”手术图解案例三 | 延髓-胸段脊髓18cm巨大
- [案例]中德国际交流项目进行时|INC巴特朗菲教授顺利完成一台儿
- [案例]两位30+男性接连确诊:当「人生黄金期」遭遇「脑功能区
- [案例]长在大脑“隐秘的角落”,这个良性病变差点让孩子失去
中枢神经系统(CNS)肿瘤是儿童期最常见的实体瘤。分子检测技术,包括下一代测序(NGS)、基因组拷贝数分析、融合转录本检测和基因组DNA甲基化分析,现已成为CNS肿瘤检查中不可或缺的工具。本文相关内容基于INC国际神经外科医生集团专家、旧金山加利福尼亚大学(UCSF)神经外科系教授兼主任Mitchel S. Berger教授的研究与临床经验整理而成。
根据现行WHO指南,许多CNS肿瘤类型在没有分子检测结果的情况下无法获得可靠诊断。美国国家综合癌症网络(NCCN)指南同样将分子检测纳入CNS肿瘤诊疗指南。这些检测的费用低于CNS肿瘤患者平均总护理费用的5%,却能够持续改善治疗管理质量:提供更准确的诊断和预后判断,以及对特定治疗反应的预测。因此,常规的高级多维分子谱分析,现已成为CNS肿瘤患者标准护理所必需的检测项目。

儿童弥漫性低/高级别胶质瘤
弥漫性低级别儿童胶质瘤涵盖多种类型,包括弥漫性MYB或MYBL1改变型星形细胞瘤、血管中心性胶质瘤、多形性低级别神经上皮肿瘤,以及弥漫性MAPK通路改变型低级别胶质瘤。这类肿瘤在显微镜下呈浸润性生长,但手术后大多不易复发或扩散。
仅凭组织病理学检查无法准确预测这类肿瘤的预后,分子检测在此环节至关重要。需要注意的是,仅依靠NGS而不进行甲基化谱分析,同样可能导致误诊。从预后角度看,弥漫性儿童低级别胶质瘤整体预后较好,但CDKN2A/B纯合性缺失会增加局部复发和恶性转化的风险,建议筛查基因组拷贝数变异,以便尽早识别高风险病例。分子检测还能帮助患儿免于接受不必要的毒性治疗,对是否需要放化疗的评估具有重要参考价值。
高级别儿童弥漫性胶质瘤则包括H3 K27改变型弥漫中线胶质瘤、H3 G34突变型弥漫性半球胶质瘤、H3和IDH野生型弥漫性儿童型高级别胶质瘤,以及婴儿型半球胶质瘤(ITHG)。分子特征方面,K27突变型中线胶质瘤几乎不携带MGMT启动子甲基化,G34突变型胶质瘤通常具有MGMT启动子甲基化,部分K27改变型中线胶质瘤还包含激活的BRAF或FGFR1变体,与更长的生存期相关。婴儿型半球胶质瘤含有IDH野生型胶质母细胞瘤中最常见的遗传改变,涉及PDGFRA、MET、MYCN或NF1的改变,具有独特的基因组DNA甲基化模式,仅由受体酪氨酸激酶(RTK)激活融合驱动,对任何被激活的RTK的靶向抑制高度敏感,最常见的靶点包括NTRK1-3、ALK或ROS1。
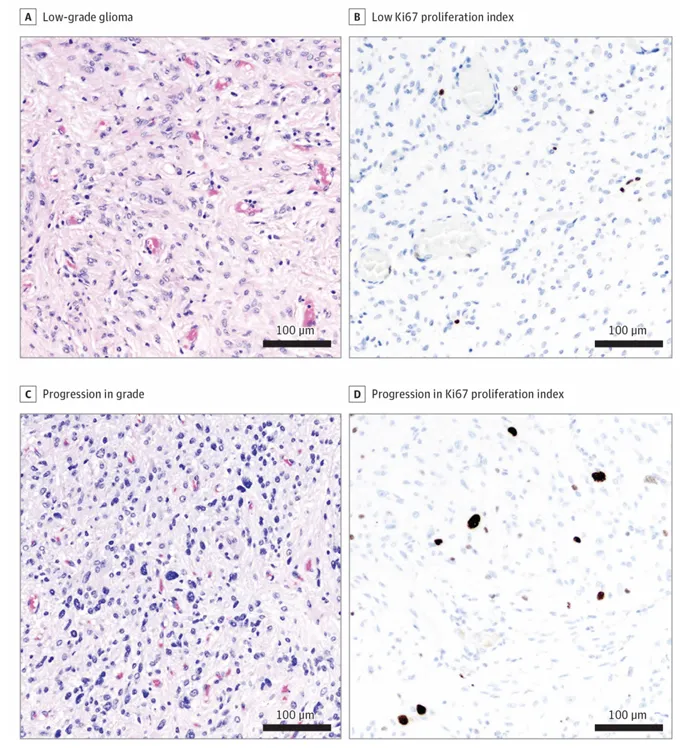
松果体区肿瘤,后经手术切除。最初诊断为低级胶质瘤,Ki67增殖指数低。但下一代测序显示肿瘤在BRAF中发生了H3-3A K27M变异和K601N变异。
局限性星形细胞胶质瘤
此类肿瘤包括毛细胞型星形细胞瘤、多形性黄色星形细胞瘤(PXA)、室管膜下巨细胞星形细胞瘤,以及脊索样胶质瘤。先进的分子诊断能够有效区分这些肿瘤与浸润性胶质瘤,从而显著改变患者的预后判断和总体治疗策略。
从治疗相关的分子标志物来看,PXA携带BRAF V600E突变,RAF和MEK抑制剂组合可能非常有效;毛细胞型星形细胞瘤存在BRAF融合,可采用RAF和/或MEK抑制剂治疗;室管膜下巨细胞星形细胞瘤存在mTOR激活变体,适用mTOR抑制剂治疗。此外,DNA甲基化谱分析目前被WHO分类认为是诊断HGAP的唯一可靠方法。HGAP在表现上可能类似于毛细胞型星形细胞瘤或IDH野生型胶质母细胞瘤,其预后介于两者之间——比毛细胞型星形细胞瘤差,但优于IDH野生型胶质母细胞瘤。
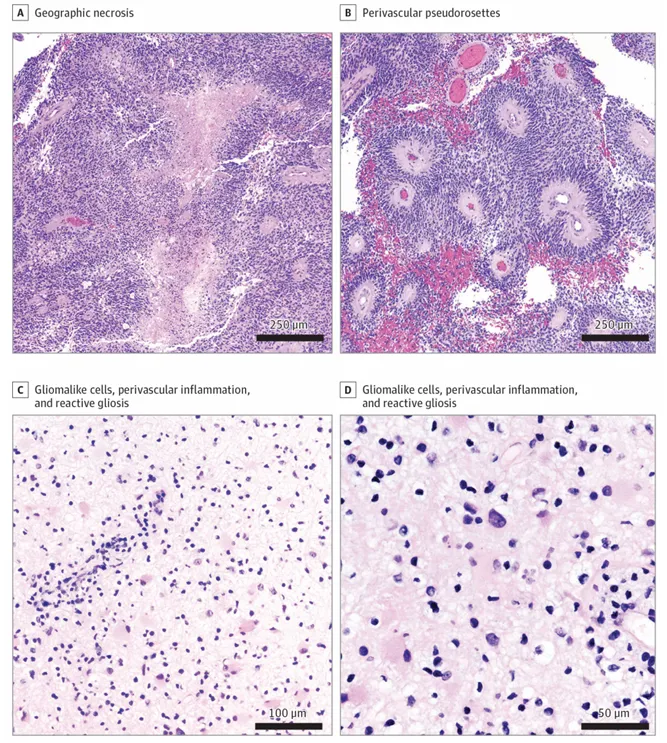
一个额叶顶骨肿块,曾被诊断为野生型胶质母细胞瘤和3级室管膜瘤,但多年后重新检查该病例时,下一代测序检测出BRAF V600E,并通过甲基化谱线性与多形黄星细胞瘤匹配。另一例中,下一代代测序、甲基化分析和融合筛查唯一检测到的异常是涉及5q21.1-5q21.3的杂合缺失。因此,最终诊断为低级别胶质瘤,建议观察等待并暂停辅助治疗,直到病变复发。
胶质神经元和神经元肿瘤
WHO分类第5版新增了3种肿瘤类型:具有少突胶质细胞瘤样特征和核团的弥漫性胶质神经元肿瘤(分子特征为14号染色体单体)、粘液样胶质神经元肿瘤(分子特征为PDGFRA的K385L或K385I变体),以及多结节和空泡性神经元肿瘤(分子特征为MAPK通路激活变体,最常见涉及MAP2K1)。
室管膜瘤
WHO分类第5版对室管膜瘤进行了分子分型。幕上室管膜瘤的名称中即包含特定分子改变——ZFTA或YAP1融合,这一分子信息有助于将其与FOXR2驱动或BCOR驱动的胚胎性肿瘤区分开来,也有助于与MN1改变的星母细胞瘤进行鉴别。
后颅窝室管膜瘤分为A组和B组,DNA甲基化谱分析是分型的决定性方法。A组肿瘤难以完全切除,B组肿瘤侵袭性较低,复发时仍可再次治疗。对于后颅窝室管膜瘤,筛查TERT启动子变体、6q染色体丢失和1q染色体获得,有助于规划辅助治疗方案和MRI监测频率。
脊髓室管膜瘤总体比幕上或后颅窝室管膜瘤更具良性特征,但携带MYC或MYCN扩增的肿瘤行为更具恶性。粘液乳头状室管膜瘤具有独特的DNA甲基化谱,可在脊髓周围扩散,在WHO分类中已从CNS 1级升级为2级。室管膜下瘤仍为CNS 1级,在组织学上可能类似于CNS 2级室管膜瘤,通过分子检测识别这一类型,可以避免不必要的术后放疗。
髓母细胞瘤
髓母细胞瘤分为四大分子亚型。WNT激活型对辅助治疗高度敏感,在儿童患者中尤为明显。SHH激活型中,TP53野生型预后为中等,TP53变体型则比无TP53变体者侵袭性强得多。非WNT/非SHH肿瘤至少包含8种不同甲基化模式,其中第6和第7亚组预后较好,第2和第3亚组预后较差,MYC(可能还有MYCN)扩增是不良预后的重要标志物。目前已有临床试验正在测试针对WNT激活型髓母细胞瘤儿童患者降低剂量的颅脊髓放疗和较低强度化疗方案。
颅咽管瘤
颅咽管瘤的两种组织学类型各具明确的分子特征:造釉质型携带CTNNB1基因变体,WNT信号通路组成性激活;乳头型则携带BRAF V600E变体,对BRAF和MEK抑制剂组合高度敏感。区分这两种亚型,并确认乳头型颅咽管瘤中的BRAF V600E突变状态,对于降低复发率和指导临床治疗决策具有重要意义。
关于Mitchel S. Berger教授
本文涉及的分子检测与儿童脑瘤预后研究,由INC国际神经外科医生集团专家、旧金山加利福尼亚大学(UCSF)神经外科系教授兼主任Mitchel S. Berger教授深度参与。Berger教授在脑肿瘤分子诊疗领域享有国际盛誉,其团队的研究为推动儿童脑瘤精准诊疗的发展作出了重要贡献。


- 所属栏目:脑瘤诊断
- 如想转载“儿童有必要做全套分子检测吗?它如何影响各类脑瘤的预后?”请务必注明来源和链接。
- 网址:https://www.incsg.com/naoliu/zhenduan/8278.html
- 更新时间:2026-05-09 10:03:14







